
| m |
| M |
| 39g |
| 78g/mol |
| 80g-13.5g |
| 80g |
| ||
| ||


科目:高中化学 来源: 题型:
合金是建造航空母舰的主体材料。
(1) 航母升降机可由铝合金制造。
① 铝元素在周期表中的位置为 。工业炼铝的原料由铝土矿提取而得。提取过程中通入的气体为 。
② Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为 。
焊接过程中使用的保护气为 (填化学式)。
(2) 航母舰体为合金钢。
① 舰体在海水中发生的电化学腐蚀主要为 。
② 航母用钢可由低硅生铁冶炼而成,则在炼铁过程中为降低硅含量需加入的物质为 。
 (3) 航母螺旋桨主要用铜合金制造。
(3) 航母螺旋桨主要用铜合金制造。
① 80.0gCu-Al合金用酸完全溶解后,
加入过量氨水,过滤得白色沉淀
39.0g,则合金中Cu的质量分数
为 。
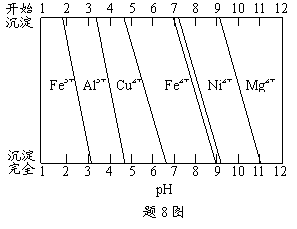
② 为分析某铜合金的成分,用酸将
其完全溶解后,用NaOH溶液调pH,当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀。结合题8图信息推断该合金中除铜外一定含有 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com