
| A. | 除①③⑤ | B. | 除③⑤⑥ | C. | ②④⑦ | D. | ①②④⑦ |
分析 ①蒸馏时,温度计测量馏分温度;
②测定某溶液的pH时,先将pH试纸放在表面皿上,再用洁净、干燥的玻璃棒蘸取该溶,液点在试纸上,并与标准比色卡比较,
③加入药品时,为防止酸液飞溅,应先加入乙醇再加入浓硫酸、最后加乙酸;
④对混合物液体加热时,为防止暴沸,要加入碎瓷片;
⑤滴定管需要用待装液润洗;
⑥加热后容器未放入干燥器中冷却,会吸收水,会导致测定的水的质量偏小;
⑦为防止液体污染,分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出.
解答 解:①蒸馏的原理:通过控制沸点的不同来实现物质的分离,所以温度计水银球要靠近蒸馏烧瓶支管口,不能插入蒸馏烧瓶液体中,故①错误;
②测溶液pH时,用玻璃棒蘸取溶液点滴到放在表面皿上的pH试纸上,并与标准比色卡比较,故②正确;
③浓硫酸溶于水放出大量的热,加入药品时,为防止酸液飞溅,应先加入乙醇再加入浓硫酸和乙酸,如先加浓硫酸会出现酸液飞溅的可能现象,故③错误;
④浓硫酸跟乙醇反应制乙烯是对混合液体加热的,为防止液体暴沸,常需加少量碎瓷片,故④正确;
⑤滴定管需要用待装液润洗,不润洗会使浓度变小,故⑤错误;
⑥加热后容器未放入干燥器中冷却,会吸收水,会导致测定的水的质量偏小,故⑥错误;
⑦为防止液体污染,分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出,故⑦正确;
故选:C.
点评 本题考查化学实验方案评价,为高频考点,侧重于学生的分析能力、实验能力和评价能力的考查,明确实验原理及基本操作规范性是解本题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 汤姆生 | B. | 卢瑟福 | C. | 玻尔 | D. | 道尔顿 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下水电离出的c(H+)•c(OH-)=1×10-20的溶液:Na+、Cl-、S2-、SO32- | |
| B. | 空气:C2H2、CO2、SO2、NO | |
| C. | 含Al3+的无色溶液:Na+、SO42-、K+、ClO-、HCO3- | |
| D. | 高锰酸钾溶液:H+、Na+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 解释或结论 |
| A | 被酸雨污染的农田及湖泊可撒石灰石粉末,减轻其危害 | 氧化钙可以与酸反应,生成盐和水 |
| B | 浓硫酸、浓盐酸暴露在空气中浓度降低 | 浓度降低原理相同 |
| C | 常温下,铁在浓硫酸中钝化 | 该过程体现了浓硫酸的强氧化性 |
| D | 向2SO2+O2?2SO3的平衡体系中,充入SO2,平衡正向移动 | V正增大,V逆减小,V正>V逆,所以平衡正向移动 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:c(Cl-)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 等浓度的下列稀溶液:①硫酸氢钠 ②乙酸钠 ③醋酸 ④碳酸氢钠 ⑤硝酸钠 ⑥苯酚钠,它们的pH由小到大排列为:③⑤①④②⑥ | |
| C. | 常温下0.1 mol/L的下列溶液 ①NH4Al(SO4)2 ②NH4Cl ③NH3•H2O ④CH3COONH4中c (NH4+)由大到小的顺序是:②>①>④>③ | |
| D. | 在25℃时,将a mol•L-1的氨水与0.01 mol•L-1的盐酸等体积混合反应时溶液中c(NH4+)=c(Cl-).用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应热和焓变的单位都是kJ | |
| B. | 如果反应是在恒温恒压条件下进行的,此时的反应热与焓变相等 | |
| C. | 任何化学反应都存在活化能,且不可能接近于零 | |
| D. | 任何化学反应的反应热均可通过实验直接测定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 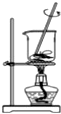 蒸发食盐水得到氯化钠晶体 | B. | 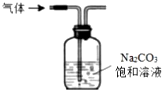 除去CO2中含有少量HCl气体 | ||
| C. | 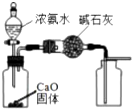 制取并收集干燥纯净的NH3 | D. |  验证SO2的还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com