
四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
| W | X | Y | Z | |
| 结构或性质 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最低负价之和为零 |
(1)Z在元素周期表中位于________族。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是________(填元素符号)。
(3)①下列可作为比较X和Y金属性强弱的依据是________(填序号)。
a.自然界中的含量 b. 单质与酸反应时失去的电子数
c.单质与水反应的难易程度 d. 最高价氧化物对应水化物的碱性
②从原子结构的角度解释X的金属性强于Y的原因: ,原子半径X>Y,所以原子核对最外层电子的吸引力X<Y,失电子能力X>Y。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物的溶液混合,反应的化学方程式是____________________________________________________
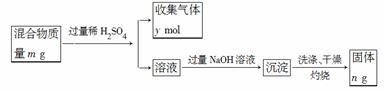
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数。能确定混合物中Y的质量分数的数据有______________(填序号)。
a.m、n b.m、y c.n、y
 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在pH=13的无色溶液中,下列各组离子能大量共存的是
A.K+、Na+、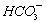 、
、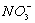 B.Na+、
B.Na+、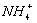 、
、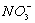 、Cl-
、Cl-
C.K+、Na+、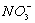 、Br- D.K+、Cu2+、Cl-、
、Br- D.K+、Cu2+、Cl-、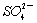
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,C0与H2反应可生成乙醇:2CO+4H2 ⇌ CH3CH20H+H20。下列关于该反应的说法错误的是
A.增大CO的浓度能减小反应速率 B.升高体系温度能增大反应速率
C.使用合适的催化剂可增大反应速率
D.若反应在密闭容器中进行,H2和C0不能全部转化为产物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.第ⅠA族的金属单质与水反应一定比第ⅡA族的金属单质剧烈
B.第二周期元素的最高正价和最低负价的绝对值之和等于8
C.同周期主族元素的原子形成简单离子的电子层结构相同
D.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
查看答案和解析>>
科目:高中化学 来源: 题型:
W、Z、Y、X四种短周期元素的原子序数依次减少。W、Z位于同周期,原子半径Z大于W;Z、W的最高正价之和等于X的最高正价;W的质子数等于X、Y的质子数之和;W的最高价氧化物对应的水化物与Z、Y的最高价氧化物对应的水化物均能发生反应。下列说法中不正确的是
A. 气态氢化物的稳定性:X<Y
B. 没有X元素也就没有丰富的有机世界
C. 非金属性Y>X,金属性W>Z
D. 在一定条件下,利用X、Z或W单质的还原性,可以冶炼某些金属
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X的最高正价和负价的绝对值之差为6,元素Y原子次外层与元素X原子次外层均为8个电子,X、Y的离子具有相同的电子排布,X、Y形成的化合物是( )
A.MgF2 B.MgCl2 C.CaCl2 D.CaBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
某甲酸溶液中含有甲醛,用下列方法可以证明的是
A.加入足量的新制氢氧化铜并加热煮沸,有砖红色的沉淀
B.加入过量的氢氧化钠充分反应后的溶液能发生银镜反应
C.将试液进行酯化反应后的混合液能发生银镜反应
D.加入足量氢氧化钠后,蒸馏出的气体通入新制的氢氧化铜悬浊液加热有砖红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,下图所示是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的工艺流程。

已知1:物质的溶解度(g/100g水) 已知2:
| 物质 | 0℃ | 40℃ | 80℃ |
| KCl | 28.0 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38.0 |
| K2Cr2O7 | 4.7 | 26.3 | 73.0 |
| Na2Cr2O7 | 163.0 | 215.0 | 376.0 |
①焙烧时有Na2CrO4、 Fe2O3 、NaAlO2 等生成。
②Cr2O72- + H2O  2CrO42- + 2H+ ;
2CrO42- + 2H+ ;
Cr2O72-具有很强的氧化性
回答问题:
(1)“浸出”步骤中,为了提高浸出率,可采取的措施有 (要求写一条)。
(2)固体b中主要含有 (填写化学式)。
(3)要检测酸化操作中溶液的pH是否等于4.5,应该使用 (填写仪器或用品名称)。
(4)酸化步骤用醋酸调节溶液的pH﹤5,其目的是 ;
不用盐酸调节溶液pH的原因是 。
(5)操作III发生反应的化学方程式是 ,
要得到K2Cr2O7 晶体的操作步骤是蒸发浓缩、冷却结晶、 、 和干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com