
Grignard试剂(卤代烃基镁)广泛运用于有机合成中,Grignard试剂的合成方法是:RX+Mg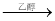 RMgX(Grignard试剂)。生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:
RMgX(Grignard试剂)。生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:
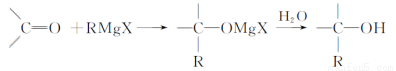
现以2-丁烯和必要的无机物为原料合成3,4-二甲基-3-己醇,进而合成一种分子式为C10H16O4的具有六元环的物质J,该物质具有对称性。合成线路如下:
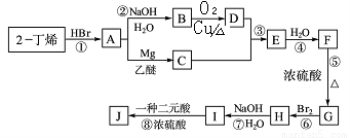
请按要求填空:
(1)用系统命名法对物质B进行命名: ;
(2)在I-J过程中所加入的二元酸的结构简式为: ;
(3)反应①~⑧中属于取代反应的有 个;属于消去反应的有 个.
A.1个 B.2个 C.3个 D.4个
(4)写出下列过程的反应方程式(有机物请用结构简式表示):
B→D ;
I→J ;
(5)写出一种满足以下条件的D的同分异构体的结构简式 。
①能与Na反应反出H2;②核磁共振氢谱有四组峰;③有二种官能团。(注:羟基不能与碳碳双键中的碳原子直接相连)
(1)2-丁醇;(2)HOOC-COOH;(3)D,A
(4)B→D
I→J: 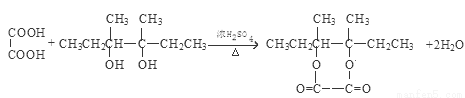
(5) 。
。
【解析】
试题分析:(1)2—丁烯CH3CH=CHCH3与HBr发生加成反应得到A:2—溴丁烷CH3CH2CHBrCH3;A与NaOH的水溶液发生取代反应得到B:2—丁醇CH3CH2CH(OH)CH3;2—丁醇在Cu存在下催化氧化得到D:丁酮 。A与Mg在乙醚存在下发生反应得到C:
。A与Mg在乙醚存在下发生反应得到C: 。C与D发生反应得到E:
。C与D发生反应得到E: ;E在水存在下反应得到F:
;E在水存在下反应得到F: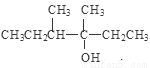 。F与浓硫酸混合加热发生消去反应得到G:
。F与浓硫酸混合加热发生消去反应得到G: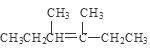 ;G与Br2发生加成反应得到H:
;G与Br2发生加成反应得到H: ;H与NaOH的水溶液混合,发生取代反应得到I:№;I与乙二酸HOOC-COOH发生酯化反应得到分子式为C10H16O4的具有对称性具有六元环的物质J
;H与NaOH的水溶液混合,发生取代反应得到I:№;I与乙二酸HOOC-COOH发生酯化反应得到分子式为C10H16O4的具有对称性具有六元环的物质J 。(1)B的系统命称为2—丁醇CH3CH2CH(OH)CH3;(2)根据在反应的过程中C守恒可知在I-J过程中所加入的二元酸是乙二酸。其结构简式为:HOOC-COOH。(3)反应①~⑧中属于取代反应的有②、④、⑦、⑧共4个;属于消去反应的有⑤共1个。(4)B→D的反应方程式为:
。(1)B的系统命称为2—丁醇CH3CH2CH(OH)CH3;(2)根据在反应的过程中C守恒可知在I-J过程中所加入的二元酸是乙二酸。其结构简式为:HOOC-COOH。(3)反应①~⑧中属于取代反应的有②、④、⑦、⑧共4个;属于消去反应的有⑤共1个。(4)B→D的反应方程式为: ;I→J的反应方程式为:
;I→J的反应方程式为:  。(5)满足条件①能与Na反应反出H2;②核磁共振氢谱有四组峰;③有二种官能团的D的同分异构体的结构简式为
。(5)满足条件①能与Na反应反出H2;②核磁共振氢谱有四组峰;③有二种官能团的D的同分异构体的结构简式为 。
。
考点:考查有机合成与推断。包括物质的结构式、结构简式、化学方程式、同分异构体的书写及反应类型的判断的知识。


科目:高中化学 来源:2013-2014学年甘肃省张掖市高三第三次诊断考试理综化学试卷(解析版) 题型:选择题
25℃时,某溶液中只含有Na+、H+、OH-、A-四种离子。下列说法正确的是 ( )
A.对于该溶液一定存在:pH≥7
B.若c(OH-)>c(H+),则溶液中不可能存在:c(Na+)>c(OH-)>c(A-)>c(H+)
C.若溶液中c(A-)= c(Na+),则溶液一定呈中性
D.若溶质为NaA,则溶液中一定存在:c(Na+)>c(A-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省天门市毕业生四月调研测试理综化学试卷(解析版) 题型:选择题
下列事实与结论(或推论)均正确的是
A.将氨水加到盛有AgCl固体的试管中,AgCl固体完全溶解,说明所得溶液中c(Ag+)·c(Cl-)>Ksp(AgCl)
B.物质的量之比为1: 2的Na2O2和NaHCO3的固体混合物,在密闭容器中充分加热反应后,残留的固体是Na2CO3
C.向FeBr2溶液中通入少量的氯气,再向反应后的溶液中滴加NaOH溶液,立即产生红褐色沉淀;那么向FeI2溶液中通入少量的氯气,也会出现同样的现象
D.将某混合气体通入品红溶液中,溶液不褪色,该气体中无Cl2
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河北省唐山市高三4月第二次模拟理综化学试卷(解析版) 题型:填空题
W、M、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质是大气污染物监测物之一;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
(1)Y3+基态的电子排布式可表示为 。
(2)MX3-的空间构型 (用文字描述)。
(3)M可形成多种氢化物,其中MH3的碱性强于M2H4的原因是 。
(4)根据等电子原理,WX分子的结构式为 。
(5)1 mol WX2中含有的σ键数目为 。
(6)H2X分子中X原子轨道的杂化类型为 。
(7)向Z2+的溶液中加入过量NaOH溶液,可生成Z的配位数为4的配位离子,写出该配位离子的结构式 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河北省唐山市高三4月第二次模拟理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,11.2 L H2O中氧原子的数目大于0.5 NA
B.6.0 g醋酸晶体中含有H+的数目为0.1 NA
C.64gCu粉与足量硫粉加热完全反应生成Cu2S时失去的电子数为2NA
D.1 mol Cl-含有的核外电子总数为8 NA
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省景德镇市高三第一次模拟考试卷理综化学试卷(解析版) 题型:填空题
A、B、C、D、E、F六种元素,其中A、B、C、D、E为短周期主族元素。它们之间的关系如下:
(Ⅰ)原子半径:A < C < B < E < D
(Ⅱ)原子的最外层电子数:A = D, C = E, A+B = C。
(Ⅲ)原子的核外电子层数:B = C = 2A
(Ⅳ)B元素的主要化合价:最高正价+最低负价 = 2
(Ⅴ)F的单质或合金是用量最大的金属材料。
请回答:(1)甲由A、B两种元素按原子数之比为3:1组成的物质,写出其电子式 ;
(2)写出某含F黑色的磁性氧化物与B最高价氧化物对应水化物的稀溶液反应的离子方程式: 。
(3)由A、C、E三种元素组成的两种气体化合物,相互反应能生成淡黄色固体的化学反应方程式为: 。
(4)上述元素中A、B、C、E、F的五种元素可形成一种常见复盐,经检测该复盐由三种离子组成且离子个数比为1:1:2,向该盐溶液加入酸化的BaCl2溶液,产生白色沉淀;加入NaOH溶液并加热,产生能使湿润红色石蕊试纸变蓝的气体,则该复盐的化学式为 。为检验该复盐中的某种有色离子存在,请写出实验的操作步骤和现象 ;
(5)将上述复盐配成0.1L 0.1mol/L的溶液,向其中加入0.06mol的BaCl2固体完全反应后,该溶液中c(SO42-)为: (已知:忽略溶液体积变化。该沉淀的Ksp=2×10-9)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省景德镇市高三第一次模拟考试卷理综化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法正确的是( )
①乙醇汽油是在汽油中加入适量乙醇作为汽车燃料,可节省石油资源,减少汽车尾气对空气的污染。
②聚乙烯塑料的老化是由于发生了加成反应。
③煤经过气化和液化等物理变化可以转化为清洁燃料。
④合成纤维、人造纤维及碳纤维都属于有机高分子材料。
⑤利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程。
⑥“地沟油”禁止食用,但可以用来制肥皂。
A.①②③ B.①④⑤ C.①⑤⑥ D.③④⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省高三百校联合调研测试(一)化学试卷(解析版) 题型:填空题
硫酸用途十分广泛,工业上合成硫酸时,将SO2转化为催化氧化是一个关键步骤。请回答下列问题:
(1)该反应在恒温恒容密闭容器中进行,判断其达到平衡状态的标志是 。(填字母)
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.容器中气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)某温度下,2SO2(g)+O2(g)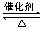 2SO3(g) △H=-196 kJ?mol-1。在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3为0.18 mol,则v(O2)= mol?L-1?min-1,放出的热量为 kJ。
2SO3(g) △H=-196 kJ?mol-1。在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3为0.18 mol,则v(O2)= mol?L-1?min-1,放出的热量为 kJ。
(3)一定温度时,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示。试分析工业生产中采用常压的原因是 。

(4)将一定量的SO2和0.7 molO2放入一定体积的密闭容器中,在550℃和催化剂作用下发生反应。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28 L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。则该反应达到平衡时SO2的转化率是多少?(要写出计算过程,计算结果保留一位小数。)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省南京市、盐城市高三第一次模拟考试化学试卷(解析版) 题型:填空题
甲酸钙广泛用于食品、化工、石油等工业生产上,300~400℃左右分解。Ⅰ、实验室制取的方法之一是:Ca(OH)2 +2HCHO + H2O2 = Ca(HCOO)2 + 2H2O + H2↑。
实验室制取时,将工业用氢氧化钙和甲醛依次加入到质量分数为30-70%的过氧化氢溶液中(投料物质的量之比依次为1∶2∶1.2),最终可得到质量分数98%以上且重金属含量极低的优质产品。
(1)过氧化氢比理论用量稍多,其目的是 。
(2)反应温度最好控制在30-70℃之间,温度不易过高,其主要原因是 。
(3)制备时在混合溶液中要加入微量硼酸钠抑制甲醛发生副反应外,还要加入少量的Na2S溶液,加硫化钠的目的是 。
(4)实验时需强力搅拌45min,其目的是 ;结束后需调节溶液的pH 7~8,其目的是 。最后经结晶分离、干燥得产品。
Ⅱ、某研究性学习小组用工业碳酸钙(主要成分为CaCO3;杂质为:Al2O3、FeCO3) 为原料,先制备无机钙盐,再与甲酸钠溶液混合制取甲酸钙。结合如图几种物质的溶解度曲线及表中相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算),现提供的试剂有:a.甲酸钠,b.5mol·L-1硝酸,c. 5mol·L-1盐酸,d. 5mol·L-1硫酸,e. 3%H2O2溶液,f.澄清石灰水。
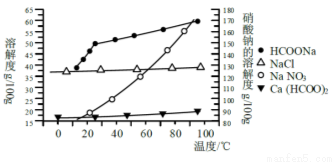
请补充完整由碳酸钙制备甲酸钙的实验步骤
金属 离子 | 开始沉淀 的pH | 沉淀完全 的pH |
Fe3+ | 1. 1 | 3. 2 |
Al3+ | 3. 0 | 5. 0 |
Fe2+ | 5. 8 | 8. 8 |
步骤1.称取13.6g甲酸钠溶于约20mL水,配成溶待用,并称取研细的碳酸钙样品10g待用。
步骤2. 。
步骤3. 。
步骤4.过滤后,将滤液与甲酸钠溶液混合,调整溶液pH 7~8,充分搅拌,所得溶液经蒸发浓缩、 、洗涤、60℃时干燥得甲酸钙晶体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com