
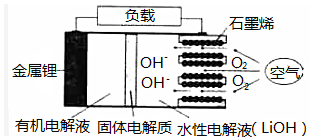
 新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )
新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )| A. | 放电时,负极反应式:Li-e-+OH-═LiOH | |
| B. | 放电时,当外电路中有1mole-转移时,水性电解液离子总数增加NA | |
| C. | 应用该电池电镀铜,阴极质量增加64g,理沦上将消耗11.2LO2 | |
| D. | 若把水性电解液换成固体氧化物电解质,则易引起正极材料碳孔堵塞 |
分析 A.放电时,负极上Li失电子得到Li+;
B.水性电解质溶液中生成氢氧根离子,同时Li+向正极移动;
C.没有说明是否是标准状况,氧气的体积无法计算;
D.电解液换成固体氧化物电解质,则正极会生成Li2O.
解答 解:A.放电时,负极上Li失电子得到Li+,则负极反应式:Li-e-═Li+,故A错误;
B.当外电路中有1mole-转移时,水性电解质溶液中生成氢氧根离子为1mol,同时Li+向正极移动1mol,则水性电解液离子总数增加2NA,故B错误;
C.没有说明是否是标准状况,气体摩尔体积不知道,所以氧气的体积无法计算,故C错误;
D.电解液换成固体氧化物电解质,则正极会生成Li2O,这样会引起碳孔堵塞,不利于正极空气的吸附,故D正确.
故选D.
点评 本题考查了原电池有关知识,侧重于考查学生的综合运用能力,题目难度中等,注意基础知识的积累掌握,掌握原电池中正负极上发生的反应为解答关键.


科目:高中化学 来源: 题型:多选题
| A. | 证明浓度的改变可导致平衡移动:将少量KCl晶体加入FeCl3+3KSC?Fe(SCN)3+3KCl的平衡体系中 | |
| B. | 除去MgCl2溶液中少量的FeCl3:向含有少量FeCl3的MgCl2溶液中加入足量的Mg(OH)2粉末,搅拌一段时间后过滤 | |
| C. | 检验某溶液中是否含有乙醛:向盛有2mL 10%CuSO4溶液的试管中滴加0.5mL10%NaOH溶液,混合均匀,滴入待检液,加热 | |
| D. | 证明Fe3+的氧化性大于I2:将KI溶液和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 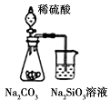 此装置可证明非金属性强弱:S>C>Si | |
| B. | 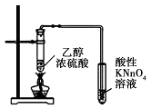 此装置可用于检验有乙烯生成 | |
| C. | 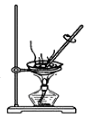 此装置可通过蒸干AlCl3饱和溶液制备AlCl3晶体 | |
| D. | 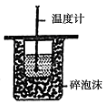 此装置可用来测定中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操 作 | 现 象 | 结 论 |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有剌激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 | Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe3+的水解平衡正向移动 |
| C | 铝片先用砂纸打磨,再加入 到浓硝酸中 | 无明显现象 | 浓硝酸具有强氧化性,常温下,铝被浓硝酸钝化 |
| D | 向等浓度的KC1、KI混合液中逐滴满加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp (AgI) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
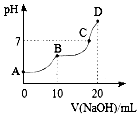 25℃时,向10mL 0.1mol•L-1 H2A溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列叙述错误的是( )
25℃时,向10mL 0.1mol•L-1 H2A溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列叙述错误的是( )| A. | C点溶液中含有NaHA和Na2A | |
| B. | NaHA溶液中水的电离程度比Na2A溶液中小 | |
| C. | B点,c (Na+)=2[c (H2A)+c (HA)+c (A2-)] | |
| D. | D点,c (Na+)>c (A2-)>c (OH-)>c (HA-)>c (H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:W>Z>X | |
| B. | X、Y、Z都能与W组成离子化合物 | |
| C. | X、Y组成的化合物可与W单质反应 | |
| D. | Q是Z、W组成的化合物,1molQ中约含有6.02×1023个阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤⑥ | B. | ②③④⑤ | C. | ①②③④⑥ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ③④⑥⑦⑧⑨ | C. | ①③⑤⑦⑧⑨ | D. | ①③②④⑥⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com