
| A£® | ZµÄ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ±ČYµÄĒæ | |
| B£® | Ō×Ó°ė¾¶£ŗr£ØW£©£¾r£ØQ£©£¾r£ØZ£©£¾r£ØX£© | |
| C£® | ÓÉX”¢Y”¢ZČżÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļæÉŅŌŹĒĖį”¢¼ī»ņŃĪ | |
| D£® | QµÄ×īøßÓŚŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļæÉŅŌČÜÓŚÅصÄYX4WČÜŅŗ |
·ÖĪö X”¢Y”¢Z”¢Q”¢WŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĪåÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£®QµÄµ„ÖŹÓėĄäĖ®·“Ó¦»ŗĀż”¢ÓėČČĖ®·“Ó¦²śÉśĘųĢ壬QĪŖMg£»Y”¢ZĶ¬ÖÜĘŚĒŅĻąĮŚ£¬X”¢QÓėY“¦ÓŚ²»Ķ¬ÖÜĘŚ£¬XĪŖH£¬YĪŖµŚ¶žÖÜĘŚŌŖĖŲ£¬Y”¢ZŌ×ӵĵē×ÓŹż×ÜŗĶÓėX”¢WŌ×ӵĵē×ÓŹż×ÜŗĶÖ®±ČĪŖ5£ŗ6£¬ÖŹ×ÓŹż=µē×ÓŹż=Ō×ÓŠņŹż£¬ÉčYµÄµē×ÓŹżĪŖx£¬ŌņZµÄµē×ÓŹżĪŖx+1£¬WµÄµē×ÓŹżĪŖy£¬Ōņ$\frac{x+x+1}{y+1}=\frac{5}{6}$£¬æÉÖŖ12x+1=5y£¬y=17£¬x=7·ūŗĻ£¬¼“YĪŖNŌŖĖŲ”¢ZĪŖOŌŖĖŲ£¬WĪŖCl£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗÓÉÉĻŹö·ÖĪöæÉÖŖ£¬XĪŖH£¬YĪŖN£¬ZĪŖO£¬QĪŖMg£¬WĪŖCl£¬
A£®·Ē½šŹōŠŌO£¾N£¬ŌņZµÄ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ±ČYµÄĒ棬¹ŹAÕżČ·£»
B£®µē×Ó²ćŌ½¶ą£¬Ō×Ó°ė¾¶Ō½“ó£¬Ķ¬ÖÜĘŚ“Ó×óĻņÓŅŌ×Ó°ė¾¶¼õŠ”£¬ŌņŌ×Ó°ė¾¶£ŗr£ØQ£©£¾r£ØW£©£¾r£ØZ£©£¾r£ØX£©£¬¹ŹB“ķĪó£»
C£®ÓÉX”¢Y”¢ZČżÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļæÉŅŌŹĒĖį”¢¼ī»ņŃĪ£¬ČēĻõĖįĪŖĖį”¢Ņ»Ė®ŗĻ°±ĪŖ¼ī”¢ĻõĖįļ§ĪŖŃĪ£¬¹ŹCÕżČ·£»
D£®QµÄ×īøßÓŚŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĪŖMg£ØOH£©2£¬æÉŅŌČÜÓŚÅصÄNH4ClČÜŅŗ£¬“Ł½ųĒāŃõ»ÆĆ¾µÄČܽāĘ½ŗāÕżĻņŅĘ¶Æ£¬¹ŹDÕżČ·£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éŌ×Ó½į¹¹ÓėŌŖĖŲÖÜĘŚĀÉ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌŖĖŲµÄĪ»ÖĆ”¢ŠŌÖŹ”¢ŌŖĖŲÖÜĘŚĀÉĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅāŌŖĖŲ»ÆŗĻĪļÖŖŹ¶µÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø
ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø æŚĖćŠÄĖćĖŁĖćÓ¦ÓĆĢāĻµĮŠ“š°ø
æŚĖćŠÄĖćĖŁĖćÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”°¼ß-20”±·É»śÉĻ“óĮæŹ¹ÓƵÄĢ¼ĻĖĪ¬ŹĒŅ»ÖÖŠĀŠĶµÄÓŠ»śøß·Ö×Ó²ÄĮĻ | |
| B£® | ”°ÉńÖŪŹ®Ņ»ŗÅ”±ÓīÖę·É“¬·µ»Ų²ÕĶā±ķĆęÖ÷ŅŖŹĒÄĶøßĪĀµÄŠĀŠĶĪŽ»ś·Ē½šŹō²ÄĮĻ | |
| C£® | ”°ĢģmŅ»ŗÅ”±ŹĒÖŠ¹śµŚŅ»øöæÕ¼äŹµŃéŹŅ£¬ĘäĢ«ŃōÄܵē³Ų°åµÄÖ÷ŅŖ²ÄĮĻŹĒ¶žŃõ»Æ¹č | |
| D£® | ”°ĮÉÄž½¢”±ÉĻÓĆÓŚ½¢ŌŲ»ś½µĀäĄ¹×čĖ÷µÄĢŲÖÖøÖĄĀ£¬ŹōÓŚŠĀŠĶĪŽ»ś·Ē½šŹō²ÄĮĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĖįÓźŅ×µ¼ÖĀĶĮČĄ½ŗĮ£Īüø½H+Ź¹ĶĮČĄĖį»Æ£¬Ó°Ļģļ§Ģ¬µŖ·ŹŗĶ¼Ų·ŹµÄÓŠŠ§ĄūÓĆ | |
| B£® | Ęū³µĪ²ĘųĪŪČ¾ĪļÖŠŗ¬ÓŠµŖµÄŃõ»ÆĪļ£¬ŹĒĘūÓĶ²»ĶźČ«Č¼ÉÕŌģ³ÉµÄ | |
| C£® | øß“æ¶ČµÄµ„¾§¹čÓĆÓŚÖĘŌģµĒŌĀ³µµÄ¹āµē³ŲŗĶ¹āµ¼ĻĖĪ¬ | |
| D£® | ĀĮ¼°ĘäŗĻ½šŹĒµēĘų”¢¹¤Ņµ”¢¼ŅĶ„¹ć·ŗŹ¹ÓĆµÄ²ÄĮĻ£¬Ķس£ÓƵē½āĀČ»ÆĀĮµÄ·½·ØÖĘČ”ĀĮ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö×ÓÖŠ¼üÄÜŌ½“󣬼ü³¤Ō½³¤£¬Ōņ·Ö×ÓŌ½ĪČ¶Ø | |
| B£® | ČéĖį·Ö×Ó[CH3-CH£ØOH£©-COOH]ÖŠÓŠ 1 øöŹÖŠŌĢ¼ĒŅ 1 mol øĆ·Ö×ÓÖŠÓŠ 11 mol ¦Ņ ¼ü | |
| C£® | PCl5·Ö×ÓÖŠPŌ×ÓŗĶClŌ×Ó×īĶā²ć¶¼Āś×ć8µē×Ó½į¹¹ | |
| D£® | H-O¼ü¼üÄÜĪŖ463 kJ/mol£¬¼“18 g H2O·Ö½ā³ÉH2ŗĶO2Ź±£¬ĻūŗÄÄÜĮæĪŖ2”Į463 kJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
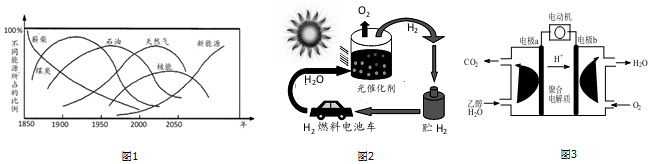
 ĪŅ¹śæĘŃŠČĖŌ±ŃŠÖĘ³öŅ»ÖÖŹŅĪĀ”°æÉŗōĪü”±Na-CO2µē³Ų£®·ÅµēŹ±øƵē³Ų”°ĪüČė”±CO2£¬³äµēŹ±”°ŗō³ö”±CO2£®ĪüČėCO2Ź±£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£®ĪüŹÕµÄČ«²æCO2ÖŠ£¬ÓŠ$\frac{2}{3}$×Ŗ»ÆĪŖNa2CO3¹ĢĢå³Į»żŌŚ¶ą±ŚĢ¼ÄÉĆ׹ܣØMWCNT£©µē¼«±ķĆę£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ĪŅ¹śæĘŃŠČĖŌ±ŃŠÖĘ³öŅ»ÖÖŹŅĪĀ”°æÉŗōĪü”±Na-CO2µē³Ų£®·ÅµēŹ±øƵē³Ų”°ĪüČė”±CO2£¬³äµēŹ±”°ŗō³ö”±CO2£®ĪüČėCO2Ź±£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£®ĪüŹÕµÄČ«²æCO2ÖŠ£¬ÓŠ$\frac{2}{3}$×Ŗ»ÆĪŖNa2CO3¹ĢĢå³Į»żŌŚ¶ą±ŚĢ¼ÄÉĆ׹ܣØMWCNT£©µē¼«±ķĆę£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | Ćæ”°ŗō³ö”±22.4LCO2£¬×ŖŅʵē×ÓŹżĪŖ$\frac{4}{3}$mol | |
| B£® | ”°ĪüČė”±CO2Ź±µÄÕż¼«·“Ó¦£ŗ4Na++3CO2+4e-=2Na2CO3+C | |
| C£® | ”°ŗō³ö”±CO2Ź±ÄĘ²µē¼«·“Ó¦Ź½ŹĒNa++e-=Na | |
| D£® | ·ÅµēŹ±µē³Ų×Ü·“Ó¦ŹĒ4Na+3CO2=2Na2CO3+C |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹÆÄ«ŗĶ½šøÕŹÆĶźČ«Č¼ÉÕ£¬ŗóÕß·ÅČȶą | |
| B£® | ½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø | |
| C£® | µČĮæµÄ½šøÕŹÆ“¢“ęµÄÄÜĮæ±ČŹÆÄ«øß | |
| D£® | ŹÆÄ«ŗÜČŻŅ××Ŗ»ÆĪŖ½šøÕŹÆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃéÄæµÄ | ŹµŃé·½°ø | |
| A | ¼ģŃéNa2SO3¾§ĢåŹĒ·ńŅŃŃõ»Æ±äÖŹ | ½«Na2SO3ѳʷČÜÓŚĻ”ĻõĖįŗ󣬵Ī¼ÓBaCl2ČÜŅŗ£¬¹Ū²ģŹĒ·ńÓŠ³ĮµķÉś³É |
| B | Ö¤Ć÷äåŅŅĶé·¢ÉśĻūČ„·“Ó¦ÓŠŅŅĻ©Éś³É | ĻņŹŌ¹ÜÖŠ¼ÓČėŹŹĮæµÄäåŅŅĶéŗĶNaOHµÄŅŅ“¼ČÜŅŗ£¬¼ÓČČ£¬½«·“Ó¦²śÉśµÄĘųĢåĶØČėäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ |
| C | ÖʱøĒāŃõ»ÆĢś½ŗĢå | Ļņ·ŠĖ®ÖŠµĪ¼ÓĀČ»ÆĢśĻ”ČÜŅŗ£¬¼ĢŠųÖó·ŠÖĮČÜŅŗ³ŹŗģŗÖÉ« |
| D | Ö¤Ć÷Mg£ØOH£©2³ĮµķæÉ×Ŗ»ÆĪŖFe£ØOH£©3³Įµķ | Ļņ2mL 1mol/L NaOHČÜŅŗÖŠĻČ¼ÓČė3µĪ1mol/L MgCl2ČÜŅŗ£¬ŌŁ¼ÓČė3µĪ1mol/L FeCl3ČÜŅŗ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com