
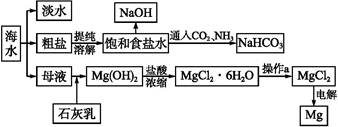
| | MgO | MgCl2 |
| 熔点/℃ | 2 852 | 714 |
| 沸点/℃ | 3 600 | 1 412 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.海洋约占地球表面积的71%,所以地球上不缺水,人类可以随意使用水资源,不必节约 |
| B.海水淡化的主要方法有蒸馏法、电渗析法和离子交换法 |
| C.海水淡化的各种方法中,蒸馏法的成本最低 |
| D.以上说法都正确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.工业上,用焦炭在电炉中还原二氧化硅得到含杂质的粗硅 |
| B.生产普通水泥的主要原料有石灰石、石英和纯碱 |
| C.工业上将粗铜电解精炼,应将粗铜连接电源的正极 |
| D.在高炉炼铁的反应中,一氧化碳作还原剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.全部 | B.只有①②③④ |
| C.只有①②③⑤ | D.只有①②④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
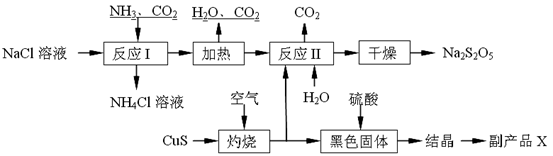
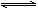 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
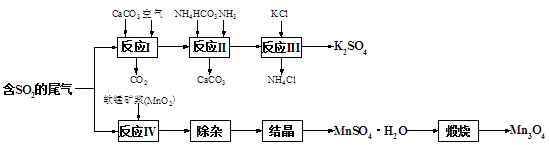
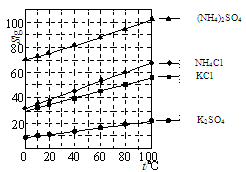

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(I)用① | B.(Ⅱ)用② | C.(Ⅲ)用③ | D.(Ⅳ)用④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com