
 ��ͼ�漰����������Ԫ���У���һ��Ԫ���⣬�����Ϊ������Ԫ�أ���֪��A��FΪ��ɫ���嵥�ʣ�BΪ��ʹʪ���ɫʯ����ֽ���������壬CΪ��ɫ�����EΪ��ɫ�������ʣ�HΪ��ɫ��Һ�����ַ�Ӧ�IJ���δ�г�������ش��������⣺
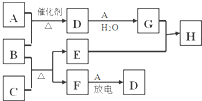
��ͼ�漰����������Ԫ���У���һ��Ԫ���⣬�����Ϊ������Ԫ�أ���֪��A��FΪ��ɫ���嵥�ʣ�BΪ��ʹʪ���ɫʯ����ֽ���������壬CΪ��ɫ�����EΪ��ɫ�������ʣ�HΪ��ɫ��Һ�����ַ�Ӧ�IJ���δ�г�������ش��������⣺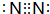 ��
������ ת����ϵ����������Ԫ���У���һ��Ԫ���⣬�����Ϊ������Ԫ�أ�BΪ��ʹʪ���ɫʯ����ֽ���������壬��BΪNH3��EΪ��ɫ�������ʣ���EΪCu��������C��Ӧ�õ�Cu��F��CΪ��ɫ�������CΪCuO��FΪ��ɫ���嵥�ʣ�ֻ��ΪN2���÷�Ӧ����ˮ���ɣ�HΪ��ɫ��Һ����Cu��G��Ӧ�õ���H����ͭ���ӣ����������嵥��A��Ӧ�õ�D��D��������ˮ��Ӧ�õ�G������֪GΪHNO3��AΪO2��DΪNO���ݴ˽��
��� �⣺ת����ϵ����������Ԫ���У���һ��Ԫ���⣬�����Ϊ������Ԫ�أ�BΪ��ʹʪ���ɫʯ����ֽ���������壬��BΪNH3��EΪ��ɫ�������ʣ���EΪCu��������C��Ӧ�õ�Cu��F��CΪ��ɫ�������CΪCuO��FΪ��ɫ���嵥�ʣ�ֻ��ΪN2���÷�Ӧ����ˮ���ɣ�HΪ��ɫ��Һ����Cu��G��Ӧ�õ���H����ͭ���ӣ����������嵥��A��Ӧ�õ�D��D��������ˮ��Ӧ�õ�G������֪GΪHNO3��AΪO2��DΪNO��
��1��������������֪��C�Ļ�ѧʽΪCuO���ʴ�Ϊ��CuO��
��2��FΪN2������ʽΪ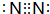 ���ʴ�Ϊ��
���ʴ�Ϊ��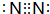 ��
��
��3��A��B��Ӧ�ǰ�����������������NO��ˮ����Ӧ��ѧ����ʽ��4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
�ʴ�Ϊ��4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
��4��Cu��ϡ���ᷴӦ��������ͭ��NO��ˮ����Ӧ���ӷ���ʽ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
�ʴ�Ϊ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
��5��ʵ�����Ʊ������Ļ�ѧ����ʽ��Ca��OH��2+2NH4Cl$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
�ʴ�Ϊ��Ca��OH��2+2NH4Cl$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
���� ���⿼��������ƶϣ����ʵ�Ԫ�����ƶ�ͻ�ƿڣ��ٽ��ת����ϵ�ƶϣ���Ҫѧ����������Ԫ�ػ������������ת�����Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
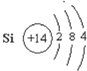 ��D��Ԫ�����ڱ��е�λ�õ�3���ڣ���VIA�壮
��D��Ԫ�����ڱ��е�λ�õ�3���ڣ���VIA�壮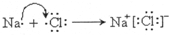 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���÷�Һ©������������Ȼ�̼ | |
| B�� | CH3COOCH3�˴Ź���������ֻ����һ���ź� | |
| C�� | �Ҵ���CH3CH2OH���Ͷ����ѣ�CH3-O-CH3����Ϊ̼���칹�� | |
| D�� | �������ӳɵõ�2��3-���������ϩ���ṹʽ��5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO��NO���������Ѫ�쵰��ϣ�ʹ���ж� | |
| B�� | CaO����SO2��Ӧ��������ҵ����������� | |
| C�� | �⻯ѧ������������������� | |
| D�� | CO2��NO2��SO2���ᵼ��������γ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH4+ Na+ OH- | B�� | Na+ H+ SO32- | ||
| C�� | K+ NO3- Cl- | D�� | Ca2+ NO3- CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ�Ľṹ��ʽ��CH2CH2 | B�� | ��ϩ�ķ���ʽ��C2H4 | ||
| C�� | ����Ľṹ��ʽ��C2H4O2 | D�� | ������ӵ����ģ���� 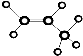 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ӷ�Һ©���Ͽڵ������ϲ�Һ���DZ���
���ӷ�Һ©���Ͽڵ������ϲ�Һ���DZ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ���� | B�� | Ũ���� | C�� | ʳ�� | D�� | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.2mol/L | B�� | 0.05mol/L | C�� | 0.45mol/L | D�� | 0.225mol/L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com