
下列与金属腐蚀有关的说法正确的是

A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu—Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2被氧化引起的
科目:高中化学 来源:2015届安徽望江中学同步课时练(人教选修4)2.1 化学反应速率试卷(解析版) 题型:选择题
在一定条件,将A2和B2两种气体通入1 L密闭容器中,发生反应:xA2(g)+yB2(g) 2C(g)。2 s内的反应速率:v(A2)=0.5 mol·L-1·s-1,v(B2)=1.5 mol·L-1·s-1,v(C)=1 mol·L-1·s-1。则x和y的值分别为( )
2C(g)。2 s内的反应速率:v(A2)=0.5 mol·L-1·s-1,v(B2)=1.5 mol·L-1·s-1,v(C)=1 mol·L-1·s-1。则x和y的值分别为( )
A.2和3 B.3和2 C.3和1 D.1和3
查看答案和解析>>
科目:高中化学 来源:2015届宁夏高三上学期第一次月考理综试卷(解析版) 题型:选择题
已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且 的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是
的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是
A.若某温度下,反应后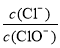 =11,则溶液中
=11,则溶液中 =
=
B.参加反应的氯气的物质的量等于 a mol
a mol
C.改变温度,产物中KClO的最大理论产量为 a mol
a mol
D.改变温度,产物中KClO3的最大理论产量为 a mol
a mol
查看答案和解析>>
科目:高中化学 来源:2015届四川省高三入学考试化学试卷(解析版) 题型:选择题
下列实验操作中不会发生安全事故的是
A.用锌粒和稀硫酸反应制取氢气,把产生的气体直接点燃,观察燃烧现象
B.把消石灰与NH4Cl固体混合加热产生的气体用导管直接通人水中制取浓氨水
C.取用少量白磷时,应在水中切割白磷,剩余的白磷立即放回原试剂瓶中
D.做完铜与浓硫酸反应实验后的试管,立即用大量水冲洗
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市高新区高三9月月考化学试卷(解析版) 题型:选择题
铁和氧化铁的混合物共a mol,加盐酸后固体全部溶解,共收集到b mol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中单质铁的物质的量为
A. molB.
molB. molC.
molC. molD.
molD. 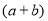 mol
mol
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市高新区高三9月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.1L1mol·L-1的NaClO 溶液中含有ClO-的数目为NA
B.78g 苯含有C=C双键的数目为3NA
C.常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA
D.标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市高新区高三9月月考化学试卷(解析版) 题型:选择题
下列化学用语正确的是
A.乙烯的分子式:CH2===CH2
B.次氯酸分子的结构式:H—O—Cl
C.羟基的电子式:
D.以铁作阳极电解时,阳极的电极反应式:Fe-3e-===Fe3+
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市2012级临诊考试化学试卷(解析版) 题型:选择题
某软质隐形眼镜材料为如下图所币的聚合物。下列有关说法错误的是

A.生成该聚合物的反应属加聚反应
B.该聚合物的单体是丙酸乙酯
C.i聚合物分子中存在大量的—OH,所以具有较好的亲水性
D.该聚合物的结构筒式为
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市元宝山区高二上学期期末化学试卷(解析版) 题型:实验题
某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室标准NaOH溶液对其进行滴定以测定它的准确浓度。下表是4种常见指示剂的变色范围:
指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
(1)该实验应选用 作指示剂。
(2)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为 mL;反应达滴定终点时的现象为 。

(3)为减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是 。
A.实验结束时,俯视刻度线读取滴定终点时NaOH溶液的体积;
B.滴定前滴定管尖嘴有气泡,滴定结束尖嘴部分充满溶液;
C.盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗;
D.锥形瓶预先用食用白醋润洗过;
E.滴加NaOH溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定。
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不用化简):C1= mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com