
�����й�Fe2��SO4��3��Һ��������ȷ���ǣ���
A�� ����Һ�У�K+��Fe2+��C6H5OH��Br﹣���Դ�������
B�� ��KI��Һ��Ӧ�����ӷ���ʽ��Fe3++2I﹣═Fe2++I2
C�� ��Ba��OH��2��Һ��Ӧ�����ӷ���ʽ��Fe3++SO42﹣+Ba2++3OH﹣═Fe��OH��3��+BaSO4��
D�� 1L O.1mol•L﹣1����Һ��������Zn��ַ�Ӧ������11.2g Fe
���㣺 ���ӹ������⣻���ӷ���ʽ����д��
ר�⣺ ���ӷ�Ӧר�⣮
������ A���������ܹ��뱽�ӷ�����ɫ��Ӧ��
B�����ݵ���غ��жϣ������ӷ���ʽ���ߵ�ɲ��غ㣻
C�������ӷ���ʽ�����������������������Ļ�ѧ��ɹ�ϵ��
D������n=cV������������������ӵ����ʵ������ٸ��������غ㼰m=nM���������������
��� �⣺A��Fe2��SO4��3��Һ�е�Fe3+��C6H5OH������ɫ��Ӧ������Һ�в��ܴ������棬��A����
B���������ܹ�������ӷ���������ԭ��Ӧ����Ӧ�����ӷ���ʽΪ��2Fe3++2I﹣═2Fe2++I2����Ŀ����ʽδ��ƽ����B����
C��Fe2��SO4��3��Һ��Ba��OH��2��Һ��Ӧ�����������������������ᱵ�����������Ӻ���������ӵ����ʵ����ı�Ϊ2��3����ȷ�����ӷ���ʽΪ��2Fe3++3SO42﹣+3Ba2++6OH﹣═2Fe��OH��3��+3BaSO4������C����
D.1L O.1mol•L﹣1����Һ�к�������������0.1mol��0.1mol�������к���0.2mol�����ӣ�������п��Ӧ��������0.2mol����������������Ϊ11.2g����D��ȷ��
��ѡD��
������ ���⿼�������ӷ���ʽ����д�����ӹ�����жϣ���Ŀ�Ѷ��еȣ�ע���������ӷ�Ӧ������������ȷ����������֮�䲻�ܹ������������ӷ���ʽ����дԭ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�CuSO4��Һ��������ȷ���ǣ�������
�� A�� ����Һ��Na+��NH4+��NO3����Mg2+���Դ�������
�� B�� ͨ��CO2���������ɫ����
�� C�� ��H2S��Ӧ�����ӷ���ʽ��Cu2++S2��=CuS��
�� D�� �����Ũ��ˮ��Ӧ�����ӷ���ʽ��Cu2++2NH3•H2O=Cu��OH��2��+2NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����л������У����е�ԭ�Ӳ����ܴ���ͬһƽ����ǣ���
A�� CH2=CH﹣CN B�� CH2=CH﹣CH=CH2
C��  D��
D�� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������һ���������ܴ������棬��������Ӧ�Լ���ᷢ����ѧ�仯�����������ӷ���ʽ��ȷ���ǣ���
ѡ�� ������ �����Լ� �����Լ�������Ӧ�����ӷ���ʽ
A Fe2+��NO3﹣��K+ ϡ���� 3Fe2++NO3﹣+4H+═3Fe3++NO��+2H2O
B Fe3+��I﹣��ClO﹣ ����������Һ Fe3++3OH﹣═Fe��OH��3��
C Ba2+��HCO3﹣��Cl﹣ ����������Һ HCO3﹣+OH﹣═CO+H2O
D Al3+��Cl﹣��NO3﹣ ��������������Һ Al3++3OH﹣═Al��OH��3��
A�� A B�� B C�� C D�� D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£����и���������ָ����Һ��һ���ܴ���������ǣ���
A�� ʹ���ȱ��ɫ����Һ��Mg2+��K+��SO42﹣��NO3﹣
B�� ʹ��̪���ɫ����Һ��Na+��Cu2+��HCO3﹣��NO3﹣
C�� 0.1 mol•L﹣1AgNO3��Һ��H+��K+��SO42﹣��I﹣
D�� 0.1 mol•L﹣1NaAlO2��Һ��H+��Na+��Cl﹣��SO42﹣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������У�����ǿ����ʵ��� ������ţ���ͬ��������������ʵ��� �����ڷǵ���ʵ��� ��
�ٰ����ڰ�ˮ������ܴ��ᣨCH3COOH�������ᱵ���Ȼ������Ȼ�����Һ�������̼�����梨�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���У�����ȷ���ǣ���
A�� ��������������Ԫ��֮һ
B�� ̼�����ƿ���������θ�����
C�� ����������ʣ����ڼ���ʳ��
D�� ʳ�ø���ά����C��ˮ�����������彡��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и������ʲ�����ͬ���칹����ǣ���
A�� 2��2﹣����������2﹣������
B�� ���ȼױ��Ͷ��ȼױ�
C�� 2﹣�����������
D�� ����ϩ��ͼ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ��װ����Ϊ���ʵ��Ŀ��ѡ�õģ�ͼ��ʵ��װ����ʵ��Ŀ����ƥ����ǣ���
A�� 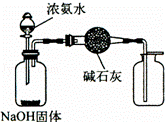
��ȡ���﴿����NH3��g��
B�� 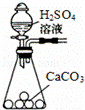
��ȡ������CO2����
C�� 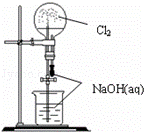
֤��Cl2����NaOH��aq����Ӧ
D�� 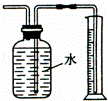
����Cu��HNO3��Ũ����Ӧ������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com