
| A. | c(Na+)=c(HA-)+2c(A2-)+c(OH-) | B. | c(H2A)+c(HA-)+c(A2-)=0.2mol•L-1 | ||
| C. | c(H+)•c(OH-)=10-14 | D. | c(A2-)+c(OH-)=c(H+)+c(H2A) |
分析 0.1mol•L-1 NaHA的强电解质溶液中,c(H+)<c(OH-),则HA-的水解大于其电离,溶液显碱性,并结合电荷守恒c(H+)+c(Na+)=c(HA-)+2c(A2-)+c(OH-)及物料守恒c(H2A)+c(HA-)+c(A2-)=0.1mol•L-1来解答.
解答 解:A.因溶液不显电性,由电荷守恒可知:c(H+)+c(Na+)=c(HA-)+2c(A2-)+c(OH-),故A错误;
B.NaHA溶液中存在的微粒有H2A、HA-、A2-,由物料守恒可知:c(H2A)+c(HA-)+c(A2-)=0.1mol•L-1,故B错误;
C.不一定为常温下,则c(H+)•c(OH-)不一定为10-14,故C错误;
D.由电荷守恒为c(H+)+c(Na+)=c(HA-)+2c(A2-)+c(OH-),物料守恒式为c(H2A)+c(HA-)+c(A2-)=c(Na+),所以c(A2-)+c(OH-)=c(H+)+c(H2A),故D正确;
故选D.
点评 本题考查离子浓度大小的比较,题目难度中等,明确NaHA的强电解质溶液中c(H+)<c(OH-)得到HA-的水解大于其电离是解答本题的关键,熟悉电荷守恒式及物料守恒式即可解答.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 将该Na2CO3 溶液转移至250ml容量瓶中,加蒸馏水稀释至刻度线,摇匀 | |
| B. | 将该Na2CO3 溶液转移至250ml烧杯中,用量筒量取150ml蒸馏水加入,搅拌 | |
| C. | 将该Na2CO3 溶液转移至250ml烧杯中,用量筒量取400ml蒸馏水加入,搅拌 | |
| D. | 将该Na2CO3 溶液转移至500ml容量瓶中,加蒸馏水稀释至刻度线,摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 碘水中通入足量的SO2:I2+SO2+2H2O=2I-+SO42-+4H+ | |
| C. | NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| D. | 惰性电极电解MgCl2溶液:Cl-+2H2O=2OH-+H2↑+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
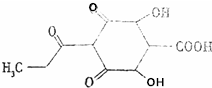 一种植物生长调节的结构简式如图所示,下列说法不正确的是( )
一种植物生长调节的结构简式如图所示,下列说法不正确的是( )| A. | 该物质含有3种官能团 | B. | 该物质属于脂环烃 | ||
| C. | 该物质属于多官能团化合物 | D. | 该物质属于烃的衍生物 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 物质的量浓度相同的盐酸和CH3COOH溶液 | |
| B. | 物质的量浓度相同的NaOH溶液和氨水 | |
| C. | pH=3的盐酸和pH=3的NH4Cl溶液均稀释100倍所得溶液 | |
| D. | pH=10的NaOH溶液和pH=10的CH3COONa溶液均稀释100倍所得溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 离子 | 物质的量浓度 |
| NH4+ | 0.4mol•L-1 |
| CO32- | 0.2mol•L-1 |
| SO42- | 0.1mol•L-1 |
| K+ | -≥0.2mol/l |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定没有甲烷 | B. | 一定没有乙烷 | ||
| C. | 可能是甲烷和乙烷的混合物 | D. | 可能是乙烷和丙烷的混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com