
 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:分析 (1)负极上燃料失电子发生氧化反应,正极得电子发生还原反应;
(2)根据化合价的变化判断氧化剂和还原剂,根据氢气和转移电子之间的关系式计算.
解答 解:(1)该反应中负极上氢气失电子生成氢离子而被氧化,所以电极反应式为H2+2OH--2e-═2H2O,正极氧气得电子发生还原反应,
电极反应式为O2+2H2O+4e-=4OH-,
故答案为:2H2+4OH--4e-=4H2O;O2+4e-+2H2O═4OH-;
(2)①LiH+H2O═LiOH+H2↑中水得电子作氧化剂,
故答案为:H2O;
②氢气的物质的量=$\frac{112L}{22.4L/mol}$=5mol,当吸收5molH2时,则生成10molLiH,10molLiH可生成10mol H2,作燃料的H2为10mol×80%=8mol,1molH2转化成1molH2O,转移2mol电子,所以8molH2可转移16mol电子,
故答案为:16.
点评 本题考查化学电源的工作原理及有关计算,题目难度较大,注意原电池电极反应式的书写以及从电子守恒的角度计算.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:选择题
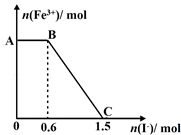 已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+,现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+,现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )| A. | 图中AB段的氧化剂为K2Cr2O7 | |
| B. | 图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 | |
| C. | 开始加入的K2Cr2O7为0.25 mol | |
| D. | 共有1molFeSO4被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 品名 | 浓缩橙汁 |
| 配料 | 水、糖、鲜橙浓缩液、柠檬酸、维生素C、β-胡萝卜素、山梨酸钾等 |
| 鲜橙原汁含量 | ≥20% |
| 净含量 | 1.5L |
| 生产日期 | 标于瓶盖上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH2+Cl2→CH2ClCH2Cl | B. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | ||
| C. | 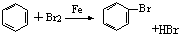 | D. | 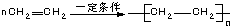 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸遇明火爆炸 | |
| B. | 浓硫酸遇水发热爆炸 | |
| C. | 铁与水反应产生的氢气接触空气遇明火爆炸 | |
| D. | 稀释后的硫酸与铁反应产生的氢气接触空气遇明火爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
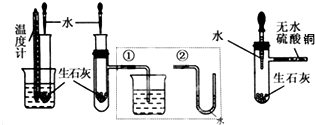
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、Al3+ | B. | Al3+ | C. | Fe2+、Al3+ | D. | NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、NH4+、Cl-、SO42- | B. | Na+、Cl-、SO42-、HCO3- | ||
| C. | Na+、CH3COO-、NO3-、K+ | D. | K+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转 | |
| B. | 能量低的电子只能在s轨道上运动,能量高的电子总是在f轨道上运动 | |
| C. | 能层序数越大,s原子轨道的半径越大 | |
| D. | 在同一能级上运动的电子,其运动状态可能相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com