
��ˮΪ�ܼ������к͵ζ���ԭ���ǣ�H3O++OH- ���� 2H2O����֪Һ̬SO2�ʹ�ˮ�ĵ����������Һ̬SO2Ҳ�ܷ����Ե��룺2SO2 ������![]() ��SO
��SO![]() +SO2+����H>0�����������д�����ǣ� ����
+SO2+����H>0�����������д�����ǣ� ����
A������Һ̬SO2Ϊ�ܼ�����SOCl2�ζ�Na2SO3���õζ���Ӧ���Ա�ʾΪ��
SO![]() +SO2+
+SO2+ 2SO2
B��Һ̬SO2���Ե���Ĵ��ڣ�˵��SO2��Һ̬ʱת��Ϊ���ӻ�����
C����һ���¶��£�Һ̬SO2��c��SO![]() ����c��SO2+���ij˻���һ������
����c��SO2+���ij˻���һ������
D���ʵ������¶ȣ�Һ̬SO2�ĵ���������ǿ

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
2- 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011��2012��߶���ѧ�ڵ�Ԫ���Ի�ѧ�Ծ������˽� ѡ���ĵ����£� ���ͣ���ѡ��
��ˮΪ�ܼ������к͵ζ���ԭ���ǣ�H3O++OH-��2H2O����֪Һ̬SO2�ʹ�ˮ�ĵ������������ΪҺ̬SO2Ҳ�ᷢ������⣺SO2��l��+SO2��l�� SO32-+SO2+������Һ̬SO2Ϊ�ܼ�����SOCl2�ζ�Cs2SO3������������������� �� ��
SO32-+SO2+������Һ̬SO2Ϊ�ܼ�����SOCl2�ζ�Cs2SO3������������������� �� ��
| A���õζ���Ӧ���Ա�ʾΪ��SO32- + SO2+��2SO2 |
| B����һ���¶��£�Һ̬SO2��c��SO32-����c��SO2+���ij˻���һ������ |
| C�������Ĵ��ڣ�˵��SO2�����ӻ����� |
| D����ͨ�����������仯���ж��Ƿ�ζ��յ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012��߶���ѧ�ڵ�Ԫ���Ի�ѧ�Ծ������˽�ѡ���ĵ����£� ���ͣ�ѡ����
��ˮΪ�ܼ������к͵ζ���ԭ���ǣ�H3O++OH-��2H2O����֪Һ̬SO2�ʹ�ˮ�ĵ������������ΪҺ̬SO2Ҳ�ᷢ������⣺SO2��l��+SO2��l��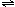 SO32-+SO2+������Һ̬SO2Ϊ�ܼ�����SOCl2�ζ�Cs2SO3������������������� �� ��
SO32-+SO2+������Һ̬SO2Ϊ�ܼ�����SOCl2�ζ�Cs2SO3������������������� �� ��
A���õζ���Ӧ���Ա�ʾΪ��SO32- + SO2+��2SO2
B����һ���¶��£�Һ̬SO2��c��SO32-����c��SO2+���ij˻���һ������
C�������Ĵ��ڣ�˵��SO2�����ӻ�����
D����ͨ�����������仯���ж��Ƿ�ζ��յ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011������ʡ�����и߿���ѧһģ�Ծ��������棩 ���ͣ�ѡ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com