
下列是A、B、C、D、E五种元素的某些性质:
|
| A | B | C | D | E |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是________。
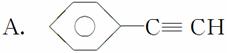
B.CH4
C.CH2===CHCH3
D.CH3CH2C≡CH
E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键___________________________________________。
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是________(化学式),理由是________________________。
(4)B、D形成的氢化物沸点:________更高,热稳定性________更强。(写化学式)
解析 (1)A是形成有机物的主要元素,所以A是碳元素,碳原子采取sp和sp3杂化方式的分子空间构型为直线形、四面体形,故D项符合题意。
(2)根据化合价可知B、D同主族,电负性D比B大,所以B是S,D是O;同理C是Cl,E是F。HF、H2O中F、O因电负性都很大,容易形成氢键,故HF之间、H2O之间以及HF和H2O之间均能形成氢键。
(3)CO2是非极性分子,SO2是极性分子,H2O是极性分子,根据“相似相溶”,SO2较易溶于水。
(4)因H2O分子间能形成氢键,H2O的沸点高于H2S;氧的非金属性强于S,故H2O比H2S更稳定。
答案 (1)D
(2)F—H…F、F—H…O、O—H…F、O—H…O
(3)SO2 CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”,SO2在H2O中的溶解度较大
(4)H2O H2O


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
碳及其化合物有广泛的用途。
(1)反应C(s)+ H2O(g) 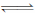 CO(g) +H2(g);ΔH= +131.3 kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
CO(g) +H2(g);ΔH= +131.3 kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
A.增加碳的用量
B.升高温度
C.用CO吸收剂除去CO
D.加入催化剂
(2)已知,C(s)+ CO2(g)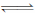 2CO(g);ΔH=+172.5kJ•mol-1,则反应 CO(g)+H2O(g)
2CO(g);ΔH=+172.5kJ•mol-1,则反应 CO(g)+H2O(g)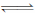 CO2(g)+H2(g)的ΔH= kJ•mol-1。
CO2(g)+H2(g)的ΔH= kJ•mol-1。
(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为 。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)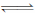 CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
①其他条件不变,降低温度,达到新平衡前v(逆)_____v(正)(填“>”、“<”或“=”)。
②该温度下,此反应的平衡常数K= 。
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数 (填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组数据中比值为2:1的是( )
A.K2SO3溶液中c(K+)与c(SO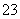 )之比
)之比
B.0.2mol·L-1的CH3COOH溶液与0.1mol·L-1的盐酸中c(H+)之比
C.pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH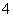 )与c(SO
)与c(SO )之比
)之比
D.pH=12的Ba(OH)2溶液与pH=12的KOH溶液中溶质的物质的量浓度之比
查看答案和解析>>
科目:高中化学 来源: 题型:
实验测得BeCl2为共价化合物,两个Be—Cl键间的夹角为180°,以下判断正确的是( )
A.由极性键构成的极性分子
B.由极性键构成的非极性分子
C.由非极性键构成的极性分子
D.BeCl2中Be采取sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
A.NH4Cl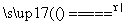 NH3↑+HCl↑
NH3↑+HCl↑
B.NH3+CO2+H2O===NH4HCO3
C.2NaOH+Cl2===NaCl+NaClO+H2O
D.2Na2O2+2CO2===2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于价层电子对互斥模型(VSEPR模型)的叙述中不正确的是( )
A.VSEPR模型可用来预测分子的立体结构
B.分子中价电子对相互排斥决定了分子的空间结构
C.中心原子上的孤电子对不参与互相排斥
D.分子中键角越大,价电子对相互排斥力越小,分子越稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,常用于水的消毒以及纺织高漂白。过氧化氢法生产亚氯酸钠的流程图如下

已知NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O且NaClO2在碱性条件下稳定性较高。试回答下列问题:
(1)在ClO2发生器中同时有氯气产生,则在发生器中发生反应的化学方程式为
(2)在NaClO2稳定装置中,H2O2作 (选填序号)。
A.氧化剂 B.还原剂
C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
(3)在实验室模拟“固体分离装置”中的技术,必须进行的实验操作是 (按实验后顺序填写操作代号)。
A.过滤 B.加热 C.分液 D.蒸馏 E.冷却
(4)经查阅资料知道:当pH≤2.0时,ClO-2能被I完全还原成Cl—;
溶液中Na2S2O3能与I2反应生成NaI和Na2S4O6。
欲测定成品中NaClO2的含量,现进行如下操作:

①步骤Ⅱ中发生反应的离子方程式是 ,
步骤Ⅲ中达到滴定终点时的现象是 。
②若上述滴定操作中用去了V mL Na2S2O3溶液,则样品中NaClO2的质量分数 (用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
有人认为人体实际上是一架缓慢氧化着的“高级机器”,人体在生命过程中也需要不断的补充“燃料”.按照这种观点,你认为人们通常摄入的下列物质不能看作“燃料”的是( )
|
| A. | 葡萄糖 | B. | 水 | C. | 油脂 | D. | 蛋白质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com