


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Ӧ��Ũ�ȣ�������λ����ڻ���ӵİٷ������Ӷ�ʹ��Ч��ײ�������� |
| B��������μӵĻ�ѧ��Ӧ��������ѹǿ������С��Ӧ������������������ӻ���ӵİٷ������Ӷ�ʹ��Ӧ�������� |
| C����C��s��+O2��g��=CO2��g����Ӧ�У�����C��������Ӧ���ʲ������� |
| D��������Ӱ�췴Ӧ��ܵ�������λ����ڻ���Ӱٷ������Ӷ�����Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������Һ�ĵ��� |
| B��ʯ���ѽ� |
| C��ú�ĸ��� |
| D�����Ȼ�̼��ȡ��ˮ�е�I2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ˮ������Ȼ��� |
| B��0.1mol/L������Һ��pHֵԼΪ3 |
| C��10mL 1mol/L����ǡ����10mL 1mol/L NaOH��Һ��ȫ��Ӧ |
| D��������Һ�����Ժ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
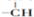 ��һ��
��һ�� ������л�����ܵĽṹ�У������������칹����������
������л�����ܵĽṹ�У������������칹����������| A��2�� | B��3�� | C��4�� | D��5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ���� |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��+1 | B��+2 | C��+3 | D��+4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com