
下列说法中正确的是( )
①钠在空气中燃烧生成白色的固体氧化钠
②钠投入硫酸铜溶液中有红色粉末产生
③过氧化钠可在防毒面具中做供氧剂
④铁丝在氯气中燃烧产生大量红棕色的烟
⑤氢气在氯气中燃烧能产生大量的白烟.
A. ①② B. ②③ C. ③④ D. ④⑤
考点: 钠的化学性质;氯气的化学性质;钠的重要化合物.
专题: 元素及其化合物.
分析: ①钠在空气中燃烧生成淡黄色的固体;
②金属钠和盐溶液的反应,先与水的反应生成氢氧化钠和氢气,然后看氢氧化钠和盐之间是否会发生复分解反应;
③在呼吸面具和潜水艇中可用过氧化钠作为供氧剂;
④铁丝在氯气中燃烧产生大量红棕色的烟;
⑤氢气在氯气中燃烧火焰呈苍白色;
解答: 解:①钠在空气中燃烧生成淡黄色的过氧化钠,故错误;
②钠投入硫酸铜溶液中,先是金属钠和水的反应:2Na+2H2O=2NaOH+H2↑,有气泡产生,其次是生成的氢氧化钠和硫酸铜之间的反应:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,生成氢氧化铜蓝色沉淀,故错误;
③过氧化钠(Na2O2)是一种淡黄色固体,常温下可与二氧化碳反应生成碳酸钠和氧气,因而常用在防毒面具里作为供氧剂,故正确;
④铁丝在氯气中燃烧产生大量红棕色的烟,产生氯化铁,故正确;
⑤氢气在氯气中燃烧火焰呈苍白色,燃烧生成氯化氢,氯化氢极易溶于水产生盐酸小液滴而在瓶口形成白雾,故错误;
故选C.
点评: 本题主要考查了物质的性质与用途,难度不大,注意物质的性质决定了物质的用途.


 小学教材全测系列答案
小学教材全测系列答案科目:高中化学 来源: 题型:
(1) (8分)某无色溶液含下列8种离子中某几种:Na+、H+、Mg2+、Ag+、Cl-、OH-、
HCO3-、NO3-。已知该溶液可与Al2O3反应,则:
① 若溶液与Al2O3反应,有Al3+生成,则溶液一定有________,一定不含有________。
② 若溶液与 Al2O3反应,有AlO2-生成,则溶液一定有________,可能含有________。
(2)(5分)有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、氯化钡溶液、碳酸钾溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,
用小试管各盛少量多次进行两两混合反应,反应现象为:A与B、A与E产生沉淀,B与D、B与E产生沉淀,C与E、D与E产生气体,而C与D无反应现象。
由此,可判定各试剂瓶中所盛试剂为:
A________,B________,C________,D________,E________。
查看答案和解析>>
科目:高中化学 来源: 题型:
德国化学家凯库勒认为,苯分子的结构中碳碳间以单、双键交替排列结合成环状.为了验证凯库勒的观点,某学生设计了以下实验方案:
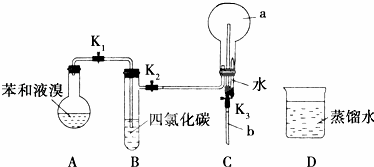
①按如图所示的装置连接好仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开K1、K2、K3止水夹;
④待烧瓶C中收集满气体后,将导管b的下端插入烧杯D里的水中,挤压预先盛有水的胶头滴管,观察实验现象.
(1)A中所发生反应的反应类型为 ,能证明凯库勒观点错误的实验现象是 .
(2)装置B的作用是 .
(3)烧瓶C的容积为500mL,收集气体时,由于空气未排尽,最终水未能充满烧瓶,假设烧瓶中混合气体对氢气的相对密度为37.9,则实验结束后,进入烧杯中的水的体积为 mL(空气的相对分子质量以29计算).
查看答案和解析>>
科目:高中化学 来源: 题型:
人们可根据物质的性质,采取适当的方式将混合物中各组分分离开来:
(1)不溶性固体与水的混合物,如BaSO4与水,可用 方法分离;
(2)可溶性固体与水的混合物,如水和食盐,可用 方法分离;
(3)两种可溶性固体,若它们的溶解度随温度变化不同,如氯化钠和硝酸钾,可通过 方法将其分离;
(4)两种互相溶解,但沸点不同的液体,如苯和四氯化碳的混合物,可用 方法分离;
(5)两种互不相溶的液体,如汽油与水,可通过 方法分离.
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏德罗常数,下列叙述正确的是( )
A. 标准状况下,22.4L H2O含有的分子数为1NA
B. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA
C. 通常状况下,1NA个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl﹣个数为1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某苯的衍生物,含有两个互为对位的取代基,其分子式为C8H10O,其中不跟NaOH溶液反应的衍生物种类有()
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
科目:高中化学 来源: 题型:
体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2(g)+O2(g)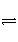
 2SO3(g)并达到平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( )
2SO3(g)并达到平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( )
A.等于p% B.大于p% C.小于p% D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室要配制500mL 0.2mol/L NaOH 溶液,请回答下列问题:
(1)配制过程中不需要使用的化学仪器有 (填字母)
A.烧杯B.容量瓶C.漏斗D.胶头滴管E.玻璃棒
(2)用托盘天平称取NaOH固体,其质量为 .
(3)下列操作步骤的正确顺序是 (填序号)
①称取一定质量的NaOH固体,放入烧杯中,用适量蒸馏水溶解;
②加蒸馏水至液面距容量瓶颈刻度线下1﹣2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转入500mL容量瓶中;
④盖好瓶盖,反复上下颠倒,摇匀;
⑤用少量的蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转入容量瓶中.
(4)若称量时耗时过长,会使配制出的NaOH溶液的物质的量浓度 (填“偏高”、“偏低”或“不变”,下同);若缺少步骤⑤,会使配制出的NaOH溶液的物质的量浓度 ,若步骤ƒ未冷却至室温就转移至容量瓶中定容,会使配制出的NaOH溶液的物质的量浓度 ;若转移时容量瓶中已有少量蒸馏水,会使配制出的NaOH溶液的物质的量浓度 ;若定容时仰视,会使配制出的NaOH溶液的物质的量浓度 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com