
 CaCO3↓+CO2↑+H2O(2分)
CaCO3↓+CO2↑+H2O(2分) MgCO3↓+CO2↑+H2O;
MgCO3↓+CO2↑+H2O; CaCO3↓+CO2↑+H2O或Mg2++2HCO3-
CaCO3↓+CO2↑+H2O或Mg2++2HCO3- MgCO3↓+CO2↑+H2O,
MgCO3↓+CO2↑+H2O,

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源:不详 题型:单选题
| A.乙醇汽油是一种纯净物 |
| B.乙醇汽油作燃料不会产生碳氧化物等有害气体,其优点是可以减少对环境的污染 |
| C.乙醇和汽油都可作溶剂,也可相互溶解 |
| D.乙醇和乙二醇互为同系物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
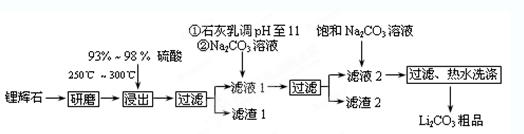
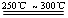 Li2SO4+Al2O3·4SiO2·H2O↓
Li2SO4+Al2O3·4SiO2·H2O↓| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
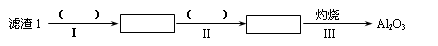
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.“可燃冰”是将水变为油的新型燃料 |
| B.氢气是具有热值高、无污染等优点的燃料 |
| C.乙醇是比汽油更环保、不可再生的燃料 |
| D.石油和煤是工厂经常使用的可再生的化石燃料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将明矾加入海水中静置过滤是海水淡化的方法之一 |
| B.海水晒盐的过程发生复分解反应 |
| C.海水中提取镁的过程不涉及氧化还原反应 |
| D.从海水中提取铀等微量元素是海水资源综合利用研究方向之一 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
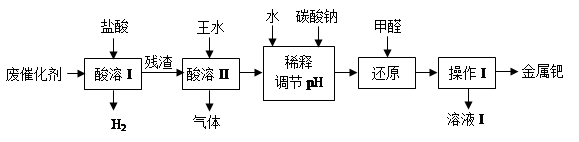
 3H2PdCl4 + 2NO↑+ 4H2O
3H2PdCl4 + 2NO↑+ 4H2O查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通过煤的直接或间接液化可以获得各种芳香烃 |
| B.通过石油的催化重整等工艺可获取芳香烃 |
| C.石油的裂化的目的主要是为了提高轻质油的产量 |
| D.石油的裂解的目的主要是为了获取不饱和烯烃 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com