
【题目】下列化学用语正确的是
①质子数为53中子数为78的碘原子:13153I
②乙烯的结构简式CH2CH2
③硫离子结构示意图: ![]()
④过氧化氢的电子式:![]()
⑤CO2的比例模型: ![]()
⑥乙醇的结构式:CH3CH2OH
⑦丙烷分子的球棍模型: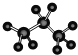
⑧T原子可以表示为31H
A.①③⑤⑥⑦⑧ B.①②③④⑦ C.①⑦⑧ D.①③⑤⑥⑦
【答案】C
【解析】
试题分析:①.碘原子质子数为53,中子数为78,质量数=质子数+中子数=131,碘原子为13153I,故①正确;②.乙烯的结构简式为CH2=CH2,故②错误;③.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构,硫离子正确的结构示意图为:![]() ,故③错误;④.过氧化氢是共价化合物,电子式为:
,故③错误;④.过氧化氢是共价化合物,电子式为:![]() ,故④错误;⑤.二氧化碳的分子式为CO2,由模型可知小球为碳原子,2个大球为氧原子,氧原子半径大,实际碳原子半径大于氧原子半径,故⑤错误;⑥.乙醇的结构简式为CH3CH2OH,其结构式为
,故④错误;⑤.二氧化碳的分子式为CO2,由模型可知小球为碳原子,2个大球为氧原子,氧原子半径大,实际碳原子半径大于氧原子半径,故⑤错误;⑥.乙醇的结构简式为CH3CH2OH,其结构式为![]() ,故⑥错误;⑦.
,故⑥错误;⑦.![]() 原子之间为单键,主链有3个碳原子,氢原子数为8个,符合丙烷的结构,故⑦正确;⑧.T原子质子数为1,中子数为2,可以表示为31H,故⑧正确;故①⑦⑧正确,答案为C。
原子之间为单键,主链有3个碳原子,氢原子数为8个,符合丙烷的结构,故⑦正确;⑧.T原子质子数为1,中子数为2,可以表示为31H,故⑧正确;故①⑦⑧正确,答案为C。


科目:高中化学 来源: 题型:
【题目】下列实验现象及所对应的离子方程式都正确的是( )

选项 | 现象 | 离子方程式 |
A | I在空气中放置一段时间后,溶液呈蓝色 | 4I-+O2+2H2O=2I2+4OH- |
B | II溶液由浅绿色变为红色 | Fe2++Cl2=Fe3++2Cl- Fe3++3SCN-=Fe(SCN)3 |
C | III溶液 颜色无变化 | Cl2+2OH- = Cl-+ClO-+H2O |
D | IV有白色沉淀生成,溶液由红色变无色 | Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.雾霾严重影响人们的生活,汽车尾气排放是造成雾霾天气的重要原因之一。已知汽车尾气排放时容易发生以下反应:
①N2(g)+O2(g)![]() 2NO(g) △H1= a kJ·mol-1
2NO(g) △H1= a kJ·mol-1
②2NO(g)+O2(g)![]() 2NO2(g) △H2= b kJ·mol-1
2NO2(g) △H2= b kJ·mol-1
③CO(g)+1/2 O2(g)![]() CO2(g) △H3= c kJ·mol-1
CO2(g) △H3= c kJ·mol-1
④2CO(g)+2NO(g)![]() N2(g)+2CO2(g) △H4
N2(g)+2CO2(g) △H4
请回答下列问题:
(1)根据反应①②③,确定反应④中△H4= kJ·mol-1。
(2)下列情况能说明反应②已达平衡状态的是 (填编号)。
A.单位时间内生成1mol NO2的同时消耗了lmol NO
B.在恒温恒容的容器中,混合气体的密度保持不变
C.混合气体的颜色保持不变
D.在恒温恒压的容器中,NO的体积分数保持不变
II.甲醇是重要的化工原料,又可作为燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下所示:
化学反应 | 平衡 常数 | 温度/℃ | ||
500 | 700 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.34 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 1.70 | 2.52 |
③3H2(g)+CO2(g) | K3 | |||
请回答下列问题:
(1)反应②是 (填“吸热”或“放热”)反应。
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3= (用K1、K2表示)。
(3)500 ℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时v正 v逆(填“>”、“=”或“<”)。
(4)反应①按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。
下列说法正确的是___________________(填序号)。
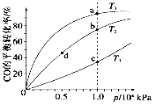
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c),v(b)>v(d)
C.平衡常数:K(a)>K(c),K(b)=K(d)
(5)新型高效的甲醇燃料电池采用铂为电极材料,两电极上分别通入CH3OH和O2。某研究小组将两个甲醇燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。回答下列问题:
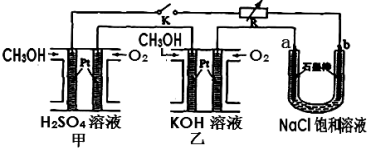
则乙燃料电池的负极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:
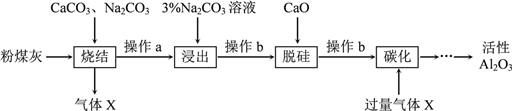
已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式_________________________。
(2)操作a为冷却、研磨,其中研磨的目的是________________________。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为_______________。
(4)操作b的名称是_________,所用的玻璃仪器有___________、__________和烧杯。
(5)“碳化”时生成沉淀,沉淀的化学式为________________。
(6)上述过程中循环使用的物质是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列元素一定属于主族元素的是
A. 位于元素周期表IIA族右边的元素
B. 原子核外最外层上有两个电子的元素
C. 原子核外最外层为8电子稳定结构的元素
D. 2010年科学家首次合成的第116号元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物的核磁共振氢谱中出现三组峰的是( )
A. CH3CH2CH2CH3 B. CH3CH2CH2OH C. CH3OCH3 D. (CH3)2CHOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药.已知:乙醚沸点为35℃.从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺为如图:
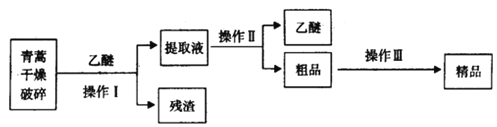
(1)对青蒿进行干燥破碎的目的是_________________________________;
(2)操作I需要的玻璃仪器主要有:烧杯、______________,操作Ⅱ的名称是______________;
(3)操作Ⅲ的主要过程可能是______________(填字母);
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
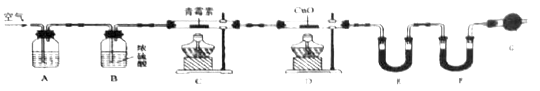
①装置A、E、F中盛放的物质分别是_________、__________、__________;
②G的作用是____________________________;
③
装置 | 实验前/g | 实验后/g |
E | 22.6 | 42.4 |
F | 80.2 | 146.2 |
则测得青蒿素的最简式是______________,欲确定其分子式,则还需要的物理量为____________;
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与______________(填字母)具有相同的性质;
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
(6)某科研小组经多次提取青蒿素实验认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如图所示:
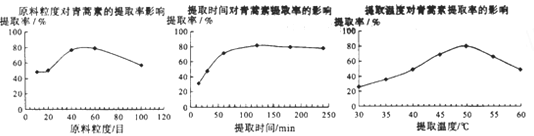
由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为______________。
A.80目、100分钟、50℃B.60目、120分钟、50℃C.60目、120分钟、55℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,若等物质的量浓度的HA溶液和NaOH溶液混合后pH=7,下列说法合理的是
A. 反应后HA溶液一定没有剩余
B. 生成物NaA的水溶液的pH可能小于7
C. HA溶液和NaOH溶液的体积可能不相等
D. HA溶液的c(H+)和NaOH溶液的c(OH-)一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由2﹣氯丙烷为主要原料制取1,2﹣丙二醇CH3CH(OH)CH2OH时,经过的反应为( )
A.加成﹣消去﹣取代 B.取代﹣加成﹣消去
C.取代﹣消去﹣加成 D.消去﹣加成﹣取代
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com