
| A. | C物质的物质的量浓度不变 | B. | 物质C和物质D的物质的量浓度相等 | ||
| C. | B物质的转化率不发生变化 | D. | 反应速率v (A)=v (D) |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、C物质的物质的量浓度不变,说明正逆反应速率相等,达平衡状态,故A正确;
B、如果AB按物质的量之比为1:2投料,则只要反应发生物质C和物质D的物质的量浓度就相等,故B错误;
C、B物质的转化率不发生变化,说明各物质的量相等,反应达平衡状态,故C正确;
D、未体现正与逆的关系,故D错误;
故选AC.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 工业上炼铁时,常用石灰石除去铁矿石中的SiO2 | |
| B. | 工业上用接触法制硫酸,在接触室里制出硫酸 | |
| C. | 工业上用二氧化硅在高温下与焦炭反应制得高纯度的硅 | |
| D. | 工业上主要从海水中提取碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 钢铁在潮湿的空气中比在干燥空气中更容易生锈 | |
| B. | 用加热蒸干AlCl3溶液的方法不能制得无水AlCl3 | |
| C. | 蒸馏水和0.1 mol•L-1NaOH溶液中的c(H+),前者大于后者 | |
| D. | 已知N2(g)+3H2(g)?2NH3(g),工业上合成氨常在高压下进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑥⑦ | B. | ③④ | C. | ③④⑦ | D. | ③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
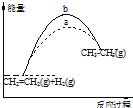
| A. | 图1的曲线说明该反应是放热反应,即CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0 | |
| B. | 化合反应都是放热反应,分解反应都是吸热反应 | |
| C. | 若图1表示有无使用催化剂时的反应进程,则b曲线使用,a曲线没使用 | |
| D. | 图中,若△H=QkJ•mol-1(Q>0),表示正反应活化能比逆反应活化能大QkJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
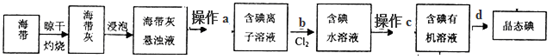
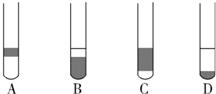
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在食盐中加入碘 | B. | 在自来水中加入碘 | ||
| C. | 在饮料中加入碘 | D. | 在饮用酒中加入碘 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com