
【题目】下列关于化学反应方向的说法正确的是
A. 凡是放热反应都是自发反应 B. 凡是熵增大的反应都是自发反应
C. 凡是吸热反应都不是自发反应 D. 反应是否自发,不只与反应热有关
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是中学常见的五种化合物。且A、B、C均含有同一种元素,A可用于呼吸面具中的氧气来源,B是制备普通玻璃的主要成分之一,D在常温下是一种常见液体,E是一种两性氢氧化物,F是一种非金属单质。它们之间有如下关系:A+D→C+F,C+E→盐+D。
(1)写出下列物质的化学式:A_____、B_____、D_____、F_______
(2)写出C+E→盐+D的离子方程式_____________________________;
(3)E中某元素的单质可与氧化铁发生铝热反应,写出其反应的化学方程式__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 2Fe2+ +Br2 = 2Fe3+ + 2Br-;2 Br- + Cl2 = Br2 + 2Cl-;2Fe3+ + 2I-= 2Fe2+ + I2。向 FeI2、FeBr2 的 混合溶液中通入 Cl2,溶液中某些离子的物质的量 n(离子)随通入 Cl2 的物质的量 n(Cl2)变化如图所示。则下列有关说法中不正确的是( )
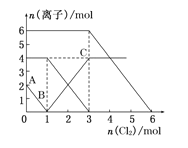
A. 还原性:I>Fe2+>Br
B. 原溶液中:n(Fe2+):n(I):n(Br)=2:1:3
C. 原混合溶液中 FeBr2 的物质的量为 6 mol
D. 当通入 2mol Cl2 时,溶液中已发生的离子反应可表示为:2Fe2++2I+2Cl2═2Fe3++I2+4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列哪种物质所含原子数与0.2 mol H3PO4所含原子数相等( )
A.0.4 mol H2O2B.0.2 mol H2SO4
C.0.9 mol NaClD.0.3 mol HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以柏林绿Fe[Fe(CN)6]为代表的新型可充电钠离子电池,其放电工作原理如图所示。下列说法错误的是

A. 放电时,正极反应为Fe[Fe(CN)6]+2Na++2e-=Na2Fe[Fe(CN)6]
B. 充电时,Mo(钼)箔接电源的负极
C. 充电时,Na+通过交换膜从左室移向右室
D. 外电路中通过0.2mol电子的电量时,负极质量变化为2.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述中正确的是( )
A.化合反应一定是氧化还原反应
B.氧化还原反应的本质是元素化合价的升降
C.金属单质在化学反应中一定作还原剂
D.失电子的反应物在反应中作还原剂,反应中被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ka(CH3COOH)=1.7×10-5,Kb(NH3·H2O)=1.7×10-5。25℃时,向40ml浓度均为0.01mol·L-1的盐酸和醋酸(1:1)混合溶液中逐滴加入0.10mol·L-1的氨水,测定过程中电导率和pH变化曲线如图所示,下列说法正确的是

A. a点溶液中,c(CH3COO-)数量级约为10-5
B. b点溶液中,c(NH4+) < c(CH3COOH)
C. c点溶液中,c(NH4+) > c(Cl-)+c(CH3COO-)
D. d点水的电离程度大于c点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com