
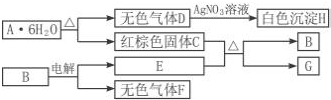
分析 AH是中学化学的常见物质,其中E、F、G是单质,B的化学式为E2F3,A的为结晶水合物加热得到无色气体D和红棕色固体C,判断C为Fe2O3,无色气体D通过硝酸银溶液会生成白色沉淀H应为AgCl沉淀,说明气体D中含氯元素,A中含铁元素、氯元素,加热得到氧化铁,说明是氯化铁溶液加热促进水解得到氢氧化铁,氢氧化铁分解得到氧化铁,气体D应为水解生成的HCl气体,G为单质,结合反应C+E=B+G分析,此反应为铝热反应,E为Al,G为Fe,B为Al2O3,F为O2,
(1)上述分析可知A为氯化铁晶体,F为氧气,H为氯化银;
(2)C和E的反应为铝热反应,铝和氧化铁高温反应生成铁和氧化铝;
(3)A•6H 2O可转化为C为氧化铁和D为HCl的原因是,加热失水,氯化铁溶解形成氯化铁溶液,加热蒸发过程中,氯化铁水解生成氢氧化铁和氯化氢,蒸发的是氯化氢气体,促进氯化铁水解正向进行,得到氢氧化铁,灼烧得到氧化铁.
解答 解:AH是中学化学的常见物质,其中E、F、G是单质,B的化学式为E2F3,A的为结晶水合物加热得到无色气体D和红棕色固体C,判断C为Fe2O3,无色气体D通过硝酸银溶液会生成白色沉淀H应为AgCl沉淀,说明气体D中含氯元素,A中含铁元素、氯元素,加热得到氧化铁,说明是氯化铁溶液加热促进水解得到氢氧化铁,氢氧化铁分解得到氧化铁,气体D应为水解生成的HCl气体,G为单质,结合反应C+E=B+G分析,此反应为铝热反应,E为Al,G为Fe,B为Al2O3,F为O2,
(1)上述分析可知A为氯化铁晶体,F为氧气,H为氯化银,化学式分别为:FeCl3•6H2O,O2 ,AgCl;
故答案为:FeCl3•6H2O;O2 ;AgCl;
(2)C和E反应的化学方程式为Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 ,
故答案为:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 ;
(3)A•6H 2O可转化为C为氧化铁和D为HCl的原因是,加热失水,氯化铁溶解形成氯化铁溶液,加热蒸发过程中,氯化铁水解生成氢氧化铁和氯化氢,蒸发的是氯化氢气体,促进氯化铁水解正向进行,得到氢氧化铁,灼烧得到氧化铁,2FeCl3•6H 2O?Fe2O3+6HCl+9H2O;HCl受热挥发,平衡右移,
故答案为:2FeCl3•6H2O?Fe2O3+6HCl+9H2O,HCl受热挥发,平衡右移.
点评 本题考查了物质转化关系的分析,物质性质和特征反应条件和反应现象是解题的突破口,掌握物质性质是关键,题目难度中等.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2→Na2CO3 | B. | FeCl3→FeCl2 | C. | H2SiO3→Na2SiO3 | D. | S→SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 利用图1所示装置吸收制取少量二氧化硫产生的尾气 | |
| B. | 利用图2所示装置制取乙烯 | |
| C. | 利用图3所示装置证明H2CO3酸性强于苯酚 | |
| D. | 利用图4所示装置制备乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. | A、B、C都不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中,pH的大小关系:②>①>③ | |
| B. | 常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7:c(Na+)>c(CH3COO-)>c(Cl-)=c(CH3COOH)>c(H+)=c(OH-) | |
| C. | 将lmolNaClO和2molNaHC03配制成1L混合溶液:c(HClO)+c(ClO-)=2c(HClO3-)+2c(H2CO3)+2c(CO32-) | |
| D. | 浓度均为0.1mol/L的NH3•H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则溶液中:C(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com