解:(1)依据题干信息,磷化铝和水反应,水解生成PH
3和氢氧化铝,反应的化学方程式为:AlP+3H
2O=Al(OH)
3↓+PH
3↑; 故答案为:AlP+3H
2O=Al(OH)
3↓+PH
3↑;
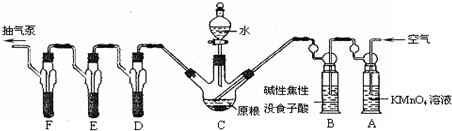
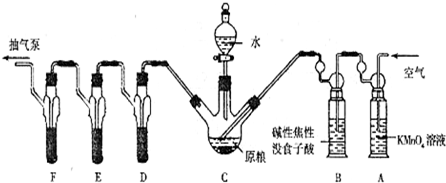
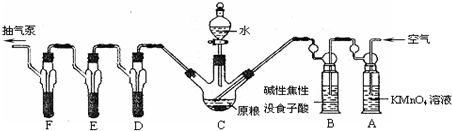
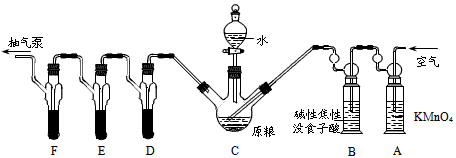
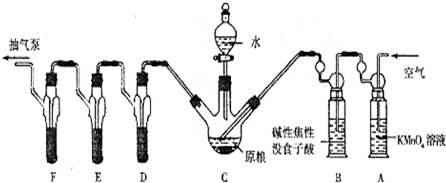
(2)利用连续装置特征,结合气体压强变化,可以利用抽气泵抽气观察各装置中气体的产生,若有气泡冒出,证明气密性完好;
故答案为:打开抽气泵抽气,观察各装置中是否有气泡产生;
(3)准确测定PH
3的含量,需要用高锰酸钾溶液全部吸收,避免产生较大误差,所以抽气泵是保证PH
3全部被吸收的措施;
故答案为:保证生成的PH
3全部被酸性KMnO
4溶液吸收;
(4)依据装置图中装置中的试剂选择分析判断,高锰酸钾溶液是强氧化剂可以吸收空气中的还原性气体;焦性没食子酸先和碱反应,再和氧气反应可以吸收氧气;若不吸收氧气,PH
3会在氧气中燃烧,用滴定方法测定的PH
3减小,结果偏低;
故答案为:还原性气体;除去空气中的O
2; 偏低;
(5)加水稀释至25mL,用浓度为5×10
-4mol/L Na
2SO
3标准溶液滴定剩余的KMnO
4溶液,消耗Na
2SO
3标准溶液11.00mL;依据滴定反应:2KMnO
4+5Na
2SO
3+3H
2SO
4=2MnSO
4+K
2SO
4+5Na
2SO
4+3H
2O;2KMnO
4~5Na
2SO
3;未反应的高锰酸钾物质的量=0.0110L×5×10
-4mol/L×
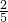
=2.2×10
-6mol;与PH
3反应的高锰酸钾物质的量=1.00×10
-3mol/L×0.0030L-2.2×10
-6mol=8.0×10
-7mol;根据反应 5PH
3+8KMnO
4+12H
2SO
4=5H
3PO
4+8MnSO
4+4K
2SO
4+12H
2O;得到定量关系为:5PH
3~8KMnO
4;计算得到PH
3物质的量=8.0×10
-7mol×
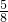
=5.0×10
-7mol;则PH
3的质量分数=
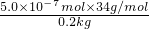
=0.085g/kg;
故答案为:0.085;
分析:(1)磷化铝能与水或酸反应产生有毒气体膦(PH
3),与水反应结合水的结构可知磷化铝能与水反应生成氢氧化铝和PH
3;
(2)依据连续装置中的压强变化分析判断;
(3)准确测定膦(PH
3)的含量需要全部吸收;
(4)高锰酸钾溶液是强氧化剂可以吸收还原性气体;碱性焦性没食子酸溶液,焦性没食子酸先和碱反应,再和氧气反应可以吸收氧气;若不吸收氧气,PH
3会在氧气中燃烧;
(5)依据消耗的亚硫酸钠物质的量结合定量关系计算剩余高锰酸钾,计算吸收PH
3需要的高锰酸钾物质的量,进一步计算PH
3物质的量,得到PH
3含量;
点评:本题以粮食中残留磷化氢的定量测定为命题背景,考查元素化合物知识氧化还原反应滴定及相关计算,综合考查了水解方程式的书写、非常规装置气密性的检验方法、实验原理的理解和定量测定的有关计算和误差分析等.

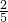 =2.2×10-6mol;与PH3反应的高锰酸钾物质的量=1.00×10-3mol/L×0.0030L-2.2×10-6mol=8.0×10-7mol;根据反应 5PH3+8KMnO4+12H2SO4=5H3PO4+8MnSO4+4K2SO4+12H2O;得到定量关系为:5PH3~8KMnO4;计算得到PH3物质的量=8.0×10-7mol×
=2.2×10-6mol;与PH3反应的高锰酸钾物质的量=1.00×10-3mol/L×0.0030L-2.2×10-6mol=8.0×10-7mol;根据反应 5PH3+8KMnO4+12H2SO4=5H3PO4+8MnSO4+4K2SO4+12H2O;得到定量关系为:5PH3~8KMnO4;计算得到PH3物质的量=8.0×10-7mol×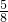 =5.0×10-7mol;则PH3的质量分数=
=5.0×10-7mol;则PH3的质量分数=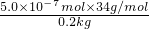 =0.085g/kg;
=0.085g/kg;