
| A. | 在测定中和反应的反应热实验中,要读取最高温度 | |
| B. | 中和滴定实验中,洗净后的锥形瓶不需要干燥 | |
| C. | 向CH3COONa溶液中滴入石蕊试液,溶液变蓝 | |
| D. | 向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS) |
分析 A.最高温度为恰好完全反应的温度;
B.中和滴定实验中,洗净后的锥形瓶不需要干燥,不影响实验结果;
C.醋酸钠是强碱弱酸盐,醋酸根离子水解导致溶液呈碱性;
D.溶度积常数大的难溶物能向溶度积常数小的难溶物转化.
解答 解:A.最高温度为恰好完全反应的温度,利用初始温度与最高温度可计算中和热,故A正确;
B.中和滴定实验中,洗净后的锥形瓶不需要干燥,不干燥只改变待测液浓度而不改变待测液中溶质的物质的量,所以不影响实验结果,故B正确;
C.醋酸钠是强碱弱酸盐,醋酸根离子水解导致溶液呈碱性,紫色石蕊试液遇碱变蓝色,故C正确;
D.溶度积常数大的难溶物能向溶度积常数小的难溶物转化,向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)>Ksp(CuS),故D错误;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及中和滴定、盐类水解、难溶物转化等知识点,明确实验原理及物质性质是解本题关键,易错选项是B,注意从操作规范性及物质性质方面解答,题目难度不大.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:解答题

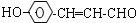 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$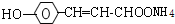 +2Ag↓+3NH3+H2O,反应类型为氧化反应
+2Ag↓+3NH3+H2O,反应类型为氧化反应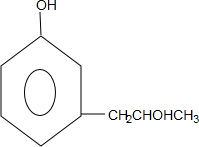 ,G的结构简式
,G的结构简式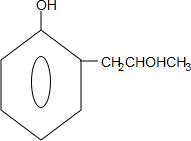 .
.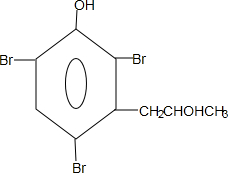 能够溶于有机物,不溶于水,所以在NaOH溶液中出现白色沉淀
能够溶于有机物,不溶于水,所以在NaOH溶液中出现白色沉淀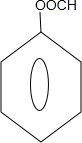 ,
,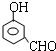 或
或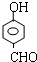 或
或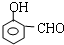 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
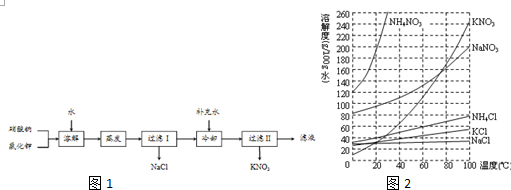
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
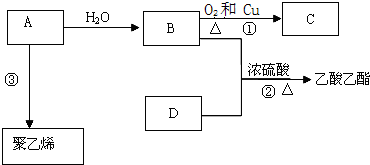
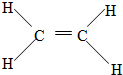 .
.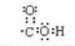 ;
;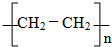 反应类型:加聚反应.
反应类型:加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁胶体滴加盐酸 | B. | 四羟基合铝酸钠溶液中加盐酸 | ||
| C. | 氯化铝溶液中滴加氢氧化钠溶液 | D. | 氯化铝溶液中滴加氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{b}$=$\frac{1}{4}$ | B. | $\frac{a}{b}$=$\frac{3}{8}$ | C. | $\frac{1}{4}$≤$\frac{a}{b}$≤$\frac{3}{8}$ | D. | $\frac{a}{b}$的值无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色、纯净的Fe(OH)2沉淀,应用如图所示电解实验可制得白色、纯净的Fe(OH)2沉淀,两电极的材料分别为石墨和铁.
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色、纯净的Fe(OH)2沉淀,应用如图所示电解实验可制得白色、纯净的Fe(OH)2沉淀,两电极的材料分别为石墨和铁.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com