
| A. | 氢氧化铯的碱性非常强 | |
| B. | 碱金属单质中铯的沸点最低 | |
| C. | 将一小块铯投入水中,实验现象与钠和水反应的完全相同 | |
| D. | 铯可以与很多非金属反应,形成离子化合物 |
分析 A.同主族从上到下,原子半径依次增大,失电子能力增强,形成碱的碱性增强;
B.金属晶体中金属原子的半径越大,金属键越弱,晶体的熔沸点越低;
C.同主族碱金属单质原子半径依次增大,失电子能力增强,和水反应的剧烈程度增强;
D.铯是活泼金属和非金属单质发生反应,通过得失电子发生反应,生成的化合物是以离子键结合.
解答 解:A.同主族从上到下,原子半径依次增大,失电子能力增强,形成碱的碱性增强,氢氧化铯的碱性强,故A正确;
B.碱金属从上到下原子半径依次增大,金属键依次减弱,单质的熔沸点依次降低,钫是放射性元素不稳定,碱金属单质中铯的沸点最低,故B正确;
C.铯活泼性大于钠,将一小块铯投入水中,铯的密度大于水,沉底剧烈反应发生燃烧或爆炸,实验现象与钠和水反应的不完全相同,故C错误;
D.铯是活泼金属和非金属单质发生反应,通过得失电子发生反应,形成的阴阳离子间形成离子键,是离子化合物,故D正确;
故选C.
点评 本题考查碱金属的性质相似性和递变规律,可以根据元素周期律知识来回答,注意递变性和差异性的分析,题目难度不大.


科目:高中化学 来源: 题型:解答题
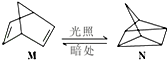
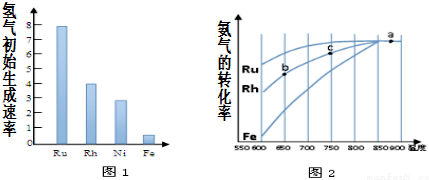
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a+b+c}{V}$mol•L-1 | B. | $\frac{a+b+2c}{V}$mol•L-1 | C. | $\frac{2a+b+c}{V}$mol•L-1 | D. | $\frac{b+2c}{V}$mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液漏斗分离水与乙醇的混合物 | |
| B. | 用激光笔检验淀粉溶液的丁达尔现象 | |
| C. | 用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液 | |
| D. | 向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6 g石墨中的C-C键数目 | |
| B. | 常温常压下,17 g ND3中所含分子数目 | |
| C. | 向含0.2 mol NH4Al(SO4)2的溶液中滴加NaOH溶液至沉淀完全溶解,消耗的OH-数目 | |
| D. | 0.1 mol羟基(-OH)中所含电子数目 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
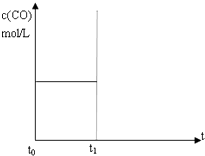 水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s)+H2O(g)?CO(g)+H2 (g)△H=+131.3kJ•mol-1
水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s)+H2O(g)?CO(g)+H2 (g)△H=+131.3kJ•mol-1查看答案和解析>>
科目:高中化学 来源: 题型:解答题
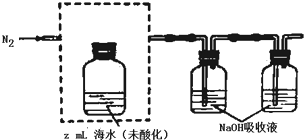
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com