
【题目】某温度下,反应2A(g)![]() B(g)(正反应为吸热反应)在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够时间后反应再次达到平衡状态,此时c(A)/c(B)=b,下列叙述正确的是( )
B(g)(正反应为吸热反应)在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够时间后反应再次达到平衡状态,此时c(A)/c(B)=b,下列叙述正确的是( )
A.在该温度下,保持容积固定不变,向容器内补充了B气体,则a<b
B.若a=b,则改变条件可能使用了催化剂
C.若其他条件不变,升高温度,则有a<b
D.若保持温度、压强不变,充入惰性气体,则有a>b
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:
【题目】已知一个可逆反应,若正反应为自发过程,则其逆反应为非自发过程,反之亦然。
(1)已知2CO(g)![]() CO2(g)+C(s),T=980 K时ΔH-TΔS=0。当体系温度低于980 K时,估计ΔH-TΔS________0(填“大于”、“小于”或“等于”,下同);当体系温度高于980 K时,估计ΔH-TΔS________0。
CO2(g)+C(s),T=980 K时ΔH-TΔS=0。当体系温度低于980 K时,估计ΔH-TΔS________0(填“大于”、“小于”或“等于”,下同);当体系温度高于980 K时,估计ΔH-TΔS________0。
(2)电子工业中清洗硅片上的SiO2(s)的反应为SiO2(s)+4HF(g)===SiF4(g)+2H2O(g) ΔH(298.15 K)=-94.0 kJ/mol,ΔS(298.15 K)=-75.8 J/(mol·K),设ΔH和ΔS不随温度而变化,则此反应自发进行的温度是________。
(3)化学反应2NO(g)+2CO(g)===N2(g)+2CO2(g)在298 K、100 kPa下:ΔH=-113.0 kJ/mol,ΔS=-145.3 J/(mol·K),反应在常温下________(填“能”或“不能”)自发进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某烷烃的相对分子质量为128,其化学式为__________________。
请根据下面给出的有关信息分析该烷烃的分子结构:若该烷烃不能由任何一种烯烃与H2发生加成反应而得到,则该烷烃的结构简式为______________________。
(2)CH3C(CH3)2CH2C(CH3)3系统命名________该烃一氯取代物有________种。
(3)支链只有一个乙基且相对分子质量最小的烷烃的结构简式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去NaCl溶液中混有的MgCl2、Na2SO4时应依次选用
A. NaOH、Ba(NO3)2、Na2CO3、HCl
B. Ca(OH)2、Mg(NO3)2、Na2CO3、HC1
C. NaOH、BaCl2、Na2CO3、HC1
D. Na2CO3、BaCl2、HC1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象正确的是( )
A.
反应的正方向放热(t1时升温)
B.
SO2气体通入氯水中
C.
NaOH溶液滴加Ca(HCO3)2溶液中
D.
将PH相同的NH4Cl溶液和稀盐酸稀释时PH的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将A与B的混合气体分别置于恒压容器甲和恒容容器乙中,发生反应:2A(g) + 2B(g)![]() 3C(g) ΔH<0。下列说法不正确的是
3C(g) ΔH<0。下列说法不正确的是

A.在相同条件下两容器内的反应均达到化学平衡状态,升温时甲、乙两容器中反应速率均增大
B.在相同条件下两容器内的反应均达到化学平衡状态,升温时甲、乙两容器中的平衡均向逆反应方向移动
C.在相同温度下,甲容器中加入2 mol A和2 mol B,乙容器中加入2 mol A和2 mol B,若甲容器中反应经30 s达到平衡状态,则乙容器中反应达到平衡所需要的时间也是30 s
D.在相同的温度和压强下,用甲容器分别进行如下反应。第一次加入2 mol A和2 mol B;第二次加入2 mol A、2 mol B和3 mol C;第三次加入4 mol C。分别达到化学平衡状态时,C的物质的量百分含量分别为X、Y、Z,则X、Y、Z的大小关系是X=Y=Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)26H2O]是分析化学中重要的试剂,学习小组探究其分解产物.
(1)甲组按照图1所示的装置进行实验,关闭止水夹并加热A中的硫酸亚铁铵固体至分解完全,检验其分解产物. 
①装置B仪器名称是 , 所放试剂是 .
②装置C中可观察到的现象是 , 由此可知硫酸亚铁铵的分解产物中有 . (写化学式)
(2)乙组选用甲组实验中的装置A和图2所示的装置进行实验验证硫酸亚铁铵分解的产物中还有SO2和SO3 . ①乙组同学的实验装置中,依次连接的合理顺序(用装置的字母表示)为A、;取适量硫酸亚铁铵固体于A中,通入一段时间N2后,关闭止水夹再点燃酒精灯,通入N2的目的是 .
②装置H中有白色沉淀,则证明分解产物中有;G中发生反应的离子方程式为 .
(3)丙组将一定量的硫酸亚铁铵在500℃时隔绝空气加热一段时间后检验其固体产物,请设计实验证明:此固体产物不含二价铁: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90.取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g.
(1)求该有机物的分子式.
(2)若该有机物呈现酸性,且该有机物的核磁共振氢谱图中出现4个吸收峰,面积比为3:1:1:1,写出其结构简式.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究碳酸钙与盐酸反应的反应速率,某同学通过如图实验装置测定反应中生成的CO2气体体积,并绘制出如图所示的曲线。请分析讨论以下问题。
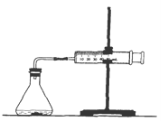
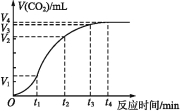
(1)化学反应速率最快的时间段是 ,影响此时间段反应速率的主要因素是 ;
A.O~t1 B.t1~t2 C.t2~t3 D.t3~t4
(2)为了减缓上述反应速率,欲向盐酸中加入下列物质,你认为可行的有 ;
A.蒸馏水 B.NaCl固体 C.NaCl溶液 D.通入HCl
(3)若盐酸的体积是20 mL,图中CO2的体积是标准状况下的体积,则t1~t2时间段平均反应速率v(HCl)= mol·(L·min)-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com