
| 时间(min) | 0 | 15 | 30 | 45 | 60 | 90 | 120 | |
| 滤纸 条的 颜色 变化 | 玻璃片I上的滤纸条 | 白色 | 白色 | 灰色 | 浅蓝色 | 蓝色 | 蓝色 | 浅蓝色 |
| 玻璃片II上的滤纸条 | 白色 | 白色 | 白色 | 白色 | 灰色 | 灰色 | 浅蓝色 | |


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
| A、CuSO4?5H2O是一种化合物 |
| B、分散系一定是混合物 |
| C、碱性氧化物不一定是金属氧化物 |
| D、氯化银、冰醋酸、酒精、水银分别属于强电解质、弱电解质、非电解质、既不是电解质也不是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
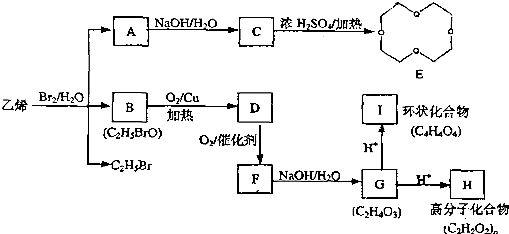
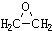 )的结构可简写为
)的结构可简写为 ,则E的分子式是
,则E的分子式是查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
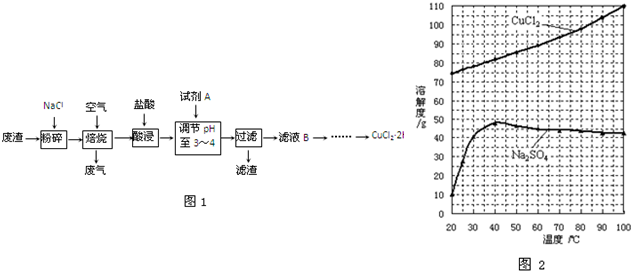
| ||
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液(mL) | 25.00 | 25.02 | 26.20 | 24.98 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | HI | H2 | I2 |
| 浓度/(mol?L-1) | 0.40 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、地下钢管连接镁块 |
| B、金属护拦表面涂漆 |
| C、枪炮表面涂上一层油 |
| D、水中的钢闸门连接电源的负极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com