
| A. | ①② | B. | ③⑥ | C. | ②④ | D. | ③⑤ |
分析 ①高锰酸根离子为有色离子,不满足溶液无色的条件;
②能使酚酞变红的溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
③加入Al能放出H2的溶液中存在大量氢离子和氢氧根离子,碳酸氢根离子与氢离子和氢氧根离子反应;
④四种离子之间不反应,为澄清透明溶液;
⑤有较多Fe3+的溶液中,铁离子与硫氰根离子、碳酸氢根离子反应;
⑥酸性溶液中,硝酸根离子能够氧化亚铁离子、碘离子.
解答 解:①无色溶液中不会存在有色的MnO4-,在溶液中不能大量共存,故①错误;
②能使酚酞变红的溶液为碱性溶液,溶液中存在大量氢氧根离子,CO32-、Na+、AlO2-、NO3-之间不发生反应,都不与氢氧根离子反应,在溶液中能够大量共存,故②正确;
③加入Al能放出H2的溶液中存在大量氢离子或氢氧根离子,HCO3-、NH4+都与氢氧根离子反应,HCO3-与氢离子反应,在溶液中一定不能大量共存,故③错误;
④某澄清溶液中:Na+、Ba2+、Cl-、Cu2+之间不发生反应,为澄清透明溶液,在溶液中能够大量共存,故④正确;
⑤有较多Fe3+的溶液中,Fe3+与SCN-、HCO3-发生反应,在溶液中不能大量共存,故⑤错误;
⑥酸性溶液中,NO3-与Fe2+、I-发生氧化还原反应,在溶液中不能大量共存,故⑥错误;
故选C.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”等.


科目:高中化学 来源: 题型:选择题
| A. | 该现象说明了NaHCO3难溶于水 | |
| B. | 滤液中的c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | 滤液中c(Na+)+c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| D. | 滤液中c(Cl-)>c(NH4+)>c(HCO3-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4 和C3H6的混合物的质量为a g,所含碳氢键数目为$\frac{a{N}_{A}}{7}$ | |
| B. | 标准状况下,2.24 L 2H35Cl 中所含中子数为1.8NA | |
| C. | 50 mL 12 mol•L-1 盐酸与足量MnO2 共热,转移的电子数为0.3NA | |
| D. | 1 L O.lmol•L-1的NaHCO3 溶液中HCO3-和CO32-的离子数之和为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
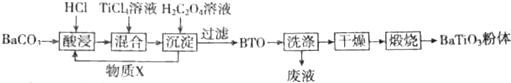
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 测定中和热时,大小两烧杯间填满碎纸的作用只是固定小烧杯 | |
| B. | 用50mL 0.50mo1•L-1的氢氧化钠溶液,分别与50mL 0.50mo1•L-1的盐酸和50mL 0.25mo1•L-1的硫酸充分反应,两反应测定的中和热相等 | |
| C. | 不能用铜丝代替玻璃棒搅拌酸碱混合液 | |
| D. | 酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1molNa2O2和22.4LCO2反应,转移电子数为1mol | |
| B. | 将钠投入到CuSO4溶液中,可以置换生成Cu | |
| C. | 将Na2O2投入到FeSO4溶液中,可生成红褐色沉淀 | |
| D. | 常温下铜与稀硫酸不反应,加入KNO3晶体后,可生成气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com