
【题目】下列说法正确的是
A. 陶瓷的主要成分是碳酸钙 B. 硅是制造半导体的常用材料
C. 电解氯化钠溶液制取金属钠 D. 用铁槽车存放浓盐酸
科目:高中化学 来源: 题型:
【题目】下列溶液中加入NaOH溶液先生成白色沉淀,沉淀迅速变灰绿色,最终变红褐色的是
A. FeSO4 B. MgSO4 C. A12(SO4)3 D. Fe2(SO4)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.按系统命名法,![]() 的名称为2,7,7-三甲基-3-乙基辛烷
的名称为2,7,7-三甲基-3-乙基辛烷
B.实验证实![]() 可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键
可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键
C. DDT的结构简式为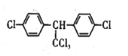 ,分子中最多有14个碳原子共平面
,分子中最多有14个碳原子共平面
D. 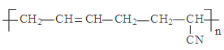 的单体是CH3-C≡C-CH3和CH2=CH-CN
的单体是CH3-C≡C-CH3和CH2=CH-CN
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将乙醇滴入热的浓硫酸中,发生反应:C2H5OH +6H2SO4 = 6SO2↑+2CO2↑+9H2O,浓硫酸没有体现的性质是
A. 氧化性 B. 脱水性 C. 酸性 D. 吸水性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Al2O3和Al(OH)3既可以与_________反应,又可以与_________反应,他们分别是_________氧化物和_________氢氧化物。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【福建省厦门市2017届高三下学期第一次质量检测理综化学试卷】某酸件废水可能含有Fe2+、Fe3+、Al3+、Mg2+、Na+、K+、CO32-、SO42-。取废水祥品分别进行如右图所示①~④四个实验。下列推断正确的是

A. 废水含有Na+,不含K+
B. 废水含有SO42-和CO32-
C. 废水不含Fe3+,可能含Fe2+
D. 废水一定含有Na+、Al3+、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次递增且都小于36的A、B、C、D、E五种元素,其中A的一种核素中没有中子,B原子基态时最外层电子数是其内层电子数的2倍,D原子基态时2p原子轨道上有2个未成对的电子,E元素的原子结构中3d能级上未成对电子数是成对电子数的2倍。回答下列问题:
(1)B2A4分子中B原子轨道的杂化类型为 ,B2A4分子中σ键和π键个数比为 。
(2)A、B、C、D四种元素的电负性从大到小的顺序为______________(用元素符号表示);化合物CA3的沸点比化合物BA4的高,其主要原因是 。
(3)元素B的一种氧化物与元素C的一种氧化物互为等电子体,元素C的这种氧化物的分子式是 。
(4)元素E能形成多种配合物,如:E(CO)5等。
①基态E原子的价电子排布图为 。
②E(CO)5常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断E(CO)5晶体属于 (填晶体类型),该晶体中E的化合价为 。
(5)E和C形成的一种化合物的晶胞结构如图所示,该晶胞的化学式为_______。若两个最近的E原子间的距离为acm,则该晶体的密度是______g·mL-1。
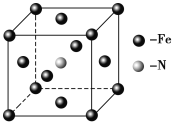
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积可变的容器中发生反应N2+3H22NH3,当增大压强使容器体积缩小时,化学反应速率加快,其主要原因是
A. 分子运动速率加快,使反应物分子间的碰撞机会增多
B. 反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C. 活化分子百分数未变,但单位体积内活化分子数增加,有效碰撞次数增多
D. 分子间距离减小,使所有的活化分子间的碰撞都成为有效碰撞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容, 4A(s)+3B(g)![]() 2C(g)+D(g)经2min,B的浓度减少0.6mol·L-1,下列说法正确的是
2C(g)+D(g)经2min,B的浓度减少0.6mol·L-1,下列说法正确的是
A. 用A表示的反应速率是0.4mol·L-1·min-1
B. 分别用B、C表示反应的速率,其关系是:3υ(B)=2υ(C)
C. 2min末的反应速率υ(B)=0.3mol·L-1·min-1
D. 气体的密度不再变化,则证明反应已经达到平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com