
(1)向含有0.1mol明矾的溶液中,逐滴加入一定浓度的NaOH溶液,当NaOH的体积是30mL和190mL时,反应体系中沉淀的质量相等,则NaOH溶液的质量的量浓度是 ;若继续加入上述NaOH溶液,当NaOH溶液的体积为 mL时,反应体系中的沉淀恰好完全溶解。
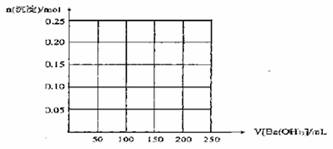
(2)如果上述明矾溶液中滴加1mol/L的Ba(OH)2溶液,请在下图中画出反应体系中产生的两种沉淀的总物质的量随Ba(OH)2溶液体积V的变化曲线。当溶液中沉淀的总物质的量最大时,沉淀的质量是 g,体系中能出现的沉淀的最大质量是 g。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:


| 实验 | 主要实验步骤及实验现象 |
| 1 | 向Y溶液中加入稀H2SO4,产生淡黄色沉淀和无色有刺激性气味的气体,该气体能使品红溶液退色. |
| 2 | 向M溶液中连续滴加Z溶液,初有白色沉淀,后沉淀溶解. |
| 3 | 向M稀溶液中滴加硝酸酸化的硝酸银溶液,产生白色沉淀. |


| 水解 |
| 水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | 主要实验步骤及实验现象 |
| 1 | 向Y溶液中加入稀H2SO4,产生淡黄色沉淀和无色有刺激性气味的气体,该气体能使品红溶液退色. |
| 2 | 向M溶液中连续滴加Z溶液,初有白色沉淀,后沉淀溶解. |
| 3 | 向M稀溶液中滴加硝酸酸化的硝酸银溶液,产生白色沉淀. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验 | 主要实验步骤及实验现象 |
| 1 | 向Y溶液中加入稀H2SO4,产生淡黄色沉淀和无色有刺激性气味的气体,该气体能使品红溶液退色. |
| 2 | 向M溶液中连续滴加Z溶液,初有白色沉淀,后沉淀溶解. |
| 3 | 向M稀溶液中滴加硝酸酸化的硝酸银溶液,产生白色沉淀. |


查看答案和解析>>
科目:高中化学 来源:2011年福建省泉州市晋江市季延中学高考化学模拟试卷(一)(解析版) 题型:解答题
| 实验 | 主要实验步骤及实验现象 |
| 1 | 向Y溶液中加入稀H2SO4,产生淡黄色沉淀和无色有刺激性气味的气体,该气体能使品红溶液退色. |
| 2 | 向M溶液中连续滴加Z溶液,初有白色沉淀,后沉淀溶解. |
| 3 | 向M稀溶液中滴加硝酸酸化的硝酸银溶液,产生白色沉淀. |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com