
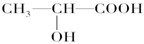
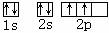
 Al Cl 1s22s22p63s23p63d104s1
Al Cl 1s22s22p63s23p63d104s1 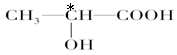 1分
1分 ;R原子的3p轨道上只有一个未成对电子,则根据构造原理可知,R原子可能是Al和Cl;Y原子的核电荷数为29,所以Y是铜元素。根据构造原理可知,其电子排布式是1s22s22p63s23p63d104s1;铜元素位于第四周期ⅠA族;区的名称来自于按照构造原理最后填入电子的能级的符号,所以铜元素属于ds区。
;R原子的3p轨道上只有一个未成对电子,则根据构造原理可知,R原子可能是Al和Cl;Y原子的核电荷数为29,所以Y是铜元素。根据构造原理可知,其电子排布式是1s22s22p63s23p63d104s1;铜元素位于第四周期ⅠA族;区的名称来自于按照构造原理最后填入电子的能级的符号,所以铜元素属于ds区。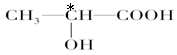 。
。

科目:高中化学 来源:不详 题型:单选题
| A.能级就是电子层 | B.每个能层最多可容纳的电子数是2n2 |
| C.同一能层中的不同能级的能量高低相同 | D.不同能层中的s能级的能量高低相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.K、Na、Li | B.Al、Mg、Na | C.N、O、C | D.Cl、S、P |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe:1s22s22p63s23p63d54s3 | B.F ˉ:1s22s22p6 |
| C.K:1s22s22p63s23p64s1 | D.Kr:1s22s22p63s23p63d104s24p6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
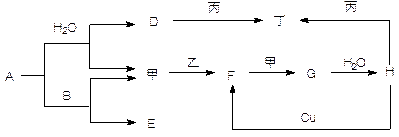
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
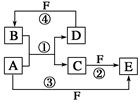
 ________________________________________。
________________________________________。 质,且反应①在水溶液中进行。
质,且反应①在水溶液中进行。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com