
【题目】室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如下图所示:
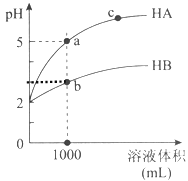
(1)HB溶液体积稀释到1000毫升时,溶液中c(H+)= mol/L。
(2)由图可判断:HA的酸性 (填“>”或“<”)HB的酸性。
(3)pH均为2的一元酸HA和HB各1mL,分别加水稀释后pH不同的原因是什么?请进行完整说明 。
【答案】
(1)10-3;(2)>;
(3)HA为强酸,HA= H++A-,加水稀释时不存在平衡的移动,n(H+)不变,c(H+)减小幅度大,pH增大幅度大;HB为弱酸,存在HB![]() H++B-,加水稀释时,电离程度增大,n(H+)增大,c(H+)减小幅度小,pH增大幅度小;
H++B-,加水稀释时,电离程度增大,n(H+)增大,c(H+)减小幅度小,pH增大幅度小;
【解析】
试题分析:(1)HB溶液体积稀释到1000毫升时,溶液的pH变为3,说明HB为弱酸,溶液中c(H+)=10-3mol/L,故答案为:10-3;
(2)加水稀释相同的倍数,HA的pH变化大于HB,说明酸性HA>HB的酸性,故答案为:>;
(3)根据图像,HA溶液体积稀释到1000毫升时,溶液的pH变为5,说明HA为强酸,HA= H++A-,加水稀释时不存在平衡的移动,n(H+)不变,c(H+)减小幅度大,pH增大幅度大;HB为弱酸,存在HB![]() H++B-,加水稀释时,电离程度增大,n(H+)增大,c(H+)减小幅度小,pH增大幅度小,故答案为:HA为强酸,HA= H++A-,加水稀释时不存在平衡的移动,n(H+)不变,c(H+)减小幅度大,pH增大幅度大;HB为弱酸,存在HB
H++B-,加水稀释时,电离程度增大,n(H+)增大,c(H+)减小幅度小,pH增大幅度小,故答案为:HA为强酸,HA= H++A-,加水稀释时不存在平衡的移动,n(H+)不变,c(H+)减小幅度大,pH增大幅度大;HB为弱酸,存在HB![]() H++B-,加水稀释时,电离程度增大,n(H+)增大,c(H+)减小幅度小,pH增大幅度小。
H++B-,加水稀释时,电离程度增大,n(H+)增大,c(H+)减小幅度小,pH增大幅度小。


科目:高中化学 来源: 题型:
【题目】下列情况中含微粒数目最多的是
A.0.5molOH—中的电子 B.1mol H2中的H原子
C.0.6mol H2SO4中的O原子 D.1molNa完全反应后失去的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁和高铁酸钾都是常见的水处理剂,下图为制备粗高铁酸钾的工业流程。
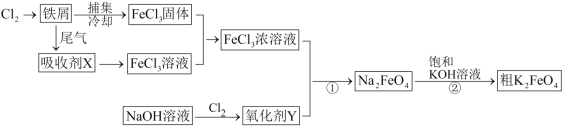
请回答下列问题:
(1)氯化铁做净水剂的原因是(结合化学用语表达) 。
(2)吸收剂X的化学式为 ,氧化剂Y的化学式为 。
(3)碱性条件下反应①的离子方程式为 。
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为2KOH+NaFeO4=K2FeO4+2NaOH,请根据反应原理分析反应能发生的原因 。
(5)K2FeO4在水溶液中易发生反应:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 (填序号)。
A.H2O B.稀KOH溶液 C.NH4Cl溶液 D.Fe(NO3)3溶液
除了这种洗涤剂外,一般工业生产还要加入异丙醇作为洗涤剂,你认为选择异丙醇的原因是 。
(6)高铁电池是正在研制中的充电电池,具有电压稳定、放电时间长等优点。以高铁酸钾、二氧化硫和三氧化硫为原料,硫酸钾为电解质,用惰性电极设计成能在高温下使用的电池,写出该电池的正极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.按系统命名法,化合物![]() 的名称是2,3,5,5-四甲基-4,4-二乙基己烷
的名称是2,3,5,5-四甲基-4,4-二乙基己烷
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C.苯和甲苯互为同系物,均能使KMnO4酸性溶液褪色
D.结构片段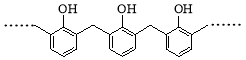 的高聚物,其单体是苯酚和甲醛
的高聚物,其单体是苯酚和甲醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关于Cl2的说法中,不正确的是
A. Cl2是一种黄绿色、密度比空气大的有毒气体
B. Cl2能与水反应生成盐酸和次氯酸
C. 工业上用Cl2和石灰水为原料制造漂白粉
D. 红热的铁丝在Cl2中剧烈燃烧,产生棕色烟
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1 mol氢约含有6.02×1023个粒子
B.H2的摩尔质量是2 g
C.1 mol O2的质量是32 g,含有的氧原子数为2NA
D.2NA个H2SO4分子的摩尔质量为196 g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一滴香”是有毒物质,被人食用后会损伤肝脏还能致癌。其分子结构如图所示,下列说法正确的是
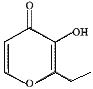
A.该有机物的分子式为C7H7O3
B.该有机物能发生取代、加成和氧化反应
C.1mol该有机物最多能与2mol H2发生加成反应
D.该有机物的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要配制2 mol/L的NaOH溶液950 mL,配制时应选用的容量瓶的规格和称取的NaOH的质量分别是( )
A.950 mL,76.0 g
B.500 mL,80.0 g
C.1 000 mL,80.0 g
D.1 000 mL,76.0 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com