
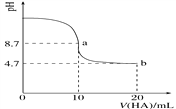
【题目】室温下向10 mL 0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )
A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b两点所示溶液中水的电离程度相同
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. b点所示溶液中c(A-)>c(HA)
【答案】D
【解析】A、a点NaOH与HA物质的量相等,则二者恰好完全反应,生成NaA,反应后溶液的pH为8.7,呈碱性,说明HA为弱酸,NaA发生水解反应,则溶液中c(Na+)>c(A-)>c(HA)>c(H+),A错误;B、a点NaA发生水解反应,促进了水的电离,b点盐酸过量,抑制水的电离,所以a点水的电离程度大于b点,B错误;C、根据电荷守恒,溶液中存在c(H+)+c(Na+)=c(OH)+c(A-),pH=7时,c(H+)=c(OH),因此溶液中:c(Na+)= c(A-),C错误;D、根据图像可知b点HA过量,因为b点溶液pH=4.7,溶液呈酸性,这说明HA的电离程度大于NaA的水解程度,所以c(A-)>c(HA),D正确,答案选D。


 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
【题目】某研究小组按下列路线合成药物胃复安:

已知: ![]()
请回答:
(1)化合物A的结构简式_______。
(2)下列说法不正确的是_______。
A.化合物B能发生加成反应 B.化合物D能与FeCl3溶液发生显色反应
C.化合物E具有碱性 D.胃复安的分子式是C13H22ClN3O2
(3)设计化合物C经两步反应转变为D 的合成路线(用流程图表示,试剂任选) _______。
(4)写出D+EF的化学方程式_______。
(5)写出化合物E可能的同分异构体的结构简式_______,须同时符合:①1H-NMR谱表明分子中有3种氢原子,IR谱显示有N一H键存在;②分子中没有同一个碳上连两个( )氮的结构。
)氮的结构。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙苯催化脱氢制苯乙烯反应:

下列说法中不正确的是( )
A. 乙苯的一氯代物共有3种不同结构
B. 苯乙烯和氢气生成乙苯的反应属于加成反应
C. 苯乙烯分子中所有原子有可能位于同一平面上
D. 等质量的苯乙烯和聚苯乙烯燃烧耗氧量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁合金可用于制笔记本电脑外壳、自行车框架等,下列叙述正确的是
A.镁合金的硬度比镁小B.镁必须密封保存
C.镁合金是电的绝缘体D.氧化膜使镁条常温下不与氧气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液中粒子浓度关系正确的是( )
A. pH=1的NaHSO4溶液:c(H+)=c(SO![]() )+c(OH-)
)+c(OH-)
B. NaHSO3溶液中c(Na+)>c(HSO)>c(OH-)>c(H+)。
C. CO2的水溶液:c(H+)>c(HCO)=2c(CO![]() )
)
D. 含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O)+c(C2O![]() )+c(H2C2O4)]
)+c(H2C2O4)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰元素在溶液中主要以Mn2+(很浅的肉色,近乎无色)、MnO42-(绿色)、MnO4-(紫色)形式存在。MnO2不溶于稀硫酸。
(1)将8 mL 0.1 mol·L-1的酸性高锰酸钾溶液和2 mL l.0mol/L的草酸(H2C2O4)溶液在试管中混合,然后将试管置于25℃水浴中,KMnO4溶液浓度随时间变化关系如下图所示。

① 写出发生反应的离子方程式:____________
② 计算前40秒用草酸表示的平均反应速率v(草酸)=________________.
③ 40s-65s的反应速率比前40s快,解释原因___________
(2)已知反应3MnO42-+2H2O![]() MnO2+2MnO4-+4OH-。
MnO2+2MnO4-+4OH-。
① 向MnO4-溶液中加入足量稀硫酸,可观察到的现象是__________.
② 常温下,在0.512 mol/L K2MnO4溶液中,当pH=14时K2MnO4的转化率为4/9,则该反应的平衡常数的值为__________
③ 在其他条件不变的条件下,适当升温有利于降低K2MnO4的转化率,则该反应的△H___0(填“大于” “小于”或“等于”)。
(3)碳酸锰是一种重要的工业原料。工业生产中常用复分解法生产MnCO3:
MnSO4+2NH4HCO3=MnCO3↓+(NH4)2SO4+CO2↑+H2O。反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8-7.4. 溶液的pH不能过低也不能过高,原因是_______。设MnSO4溶液为0.19mol/L,则溶液的pH 最高不能超过_________。
[己知MnCO3、Mn(OH)2的Ksp分别为l.8×10-11和1.9×10-13]
(4)制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中“![]() ”表示溶液中阴离子移动的方向。铂电极的电极反应式为______。
”表示溶液中阴离子移动的方向。铂电极的电极反应式为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学基本概念是化学知识的重要组成部分。
(1)在“盐析”、“ 升华”、“蒸馏”、 “干馏”这几个名词概念中,与化学变化有关联的是__________。
(2)在①氯水、②七水硫酸锌、③水玻璃、④王水这几种与“水”相关的物质概念中,表示纯净物的是_____(填写序号)
(3)“胶体”是化学基本概念之一。实验室通常采用向沸水中逐滴加入________的方法来制备Fe(OH)3胶体,生成Fe(OH)3胶体的化学方程式可表示为____________。若向所制得的Fe(OH)3胶体中逐滴加入稀硫酸至过量,可以观察到的现象是____________。
(4)“氧化还原”、“反应介质”等也是化学中常用的基本概念。重铬酸钾(K2Cr2O7)是一种比较强的氧化剂,但用它的水溶液在常温及酸性介质中与双氧水混合制备蓝色晶态CrO5的反应却是一个非氧化还原反应,请写出该反应的离子方程式______________。CrO5的名称是过氧化铬,则每个CrO5的分子中含有的过氧键数目为_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com