
下列有关电解质溶液中微粒的物质的量浓度关系正确的是双选) )。
A.在0.1 mol·L-1 NaHCO3溶液中:cNa+)>cHCO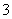 )>cCO
)>cCO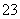 )>cH2CO3)
)>cH2CO3)
B.在0.1 mol·L-1 Na2CO3溶液中:cOH-)-cH+)=cHCO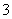 )+2cH2CO3)
)+2cH2CO3)
C.向0.2 mol·L-1 NaHCO3溶液中加入等体积0.1 mol·L-1 NaOH溶液:cCO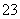 )>cHCO
)>cHCO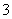 )>cOH-)>cH+)
)>cOH-)>cH+)
D.常温下,CH3COONa和CH3COOH混合溶液[pH=7,cNa+)=0.1mol·L-1]:cNa+)
=cCH3COO-)>cCH3COOH)>cH+)=cOH-)
解析 A项,在0.1 mol·L-1NaHCO3溶液中,HCO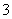 在溶液中存在水解与电离两个过程,而溶液呈碱性,说明水解程度大于电离程度,cH2CO3)>cCO
在溶液中存在水解与电离两个过程,而溶液呈碱性,说明水解程度大于电离程度,cH2CO3)>cCO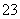 ),故错误;B项,由质子守恒关系式可知cOH-)=cH+)+cHCO
),故错误;B项,由质子守恒关系式可知cOH-)=cH+)+cHCO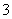 )+2cH2CO3),正确;C项,向0.2 mol·L-1 NaHCO3溶液中加入等体积0.1 mol·L-1 NaOH溶液后,相当于0.05 mol·L-1的Na2CO3溶液和0.05 mol·L-1 NaHCO3溶液,Na2CO3和NaHCO3在水中水解,CO
)+2cH2CO3),正确;C项,向0.2 mol·L-1 NaHCO3溶液中加入等体积0.1 mol·L-1 NaOH溶液后,相当于0.05 mol·L-1的Na2CO3溶液和0.05 mol·L-1 NaHCO3溶液,Na2CO3和NaHCO3在水中水解,CO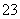 比HCO
比HCO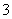 水解程度大,因此,cHCO
水解程度大,因此,cHCO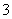 )>cCO
)>cCO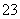 ),错误;D项,常温下,CH3COONa和CH3COOH混合溶液中,包括CH3COO-水解和CH3COOH
),错误;D项,常温下,CH3COONa和CH3COOH混合溶液中,包括CH3COO-水解和CH3COOH
电离两个过程,既然pH=7,则CH3COOH的浓度很小,cCH3COOH)<cCH3COO-),根据电荷守恒式,不难得出cNa+)=cCH3COO-) =0.1 mol·L-1,cH+)=cOH-)=1×10-7 mol·L-1,正确。
答案 BD


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
下表的实验数据是在不同温度和压强下,平衡混合物中NH3含量的变化情况。达到平衡时平衡混合物中NH3的含量(体积分数)[入料V(N2)∶V(H2)=1∶3]
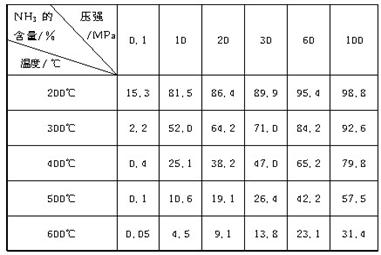
(1)比较200℃和300℃时的数据,可判断升高温度,平衡向____________方向移动,正反应方向为________(填“吸热”或“放热”)反应。
(2)根据平衡移动原理,合成氨适宜的条件是________。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
(3)计算500℃,30 MPa时N2的转化率________。
(4)实际工业生产合成氨时,考虑浓度对化学平衡的影响,还采取了一些措施。请写出其中的一个措施:________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在25℃时,将2个铜电极插入到一定的Na2SO4饱和溶液中,通直流电电解并不断搅拌,当阴极上收集到a mol气体时,溶液中析出了b mol的结晶水合物Na2SO4·10H2O,若保持温度不变,则所剩溶液中溶质的质量分数是( )
A.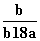 B.
B.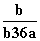 C.
C.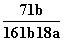 D.
D.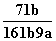
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在0.1 mol·L-1的NaHSO3溶液中有关微粒浓度由大到小的顺序为[Na+]>[HSO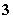 ]>[SO
]>[SO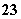 ]>[H2SO3]。
]>[H2SO3]。
(1)该溶液中[H+]________[OH-](填“>”、“<”或“=”),简述理由:
________________________________________________________________________
________________________________________________________________________。
(2)现向NH4HSO3溶液中,逐滴加入少量含有酚酞的NaOH溶液,可观察到的现象是________________________________________________________________________
________________________________________________________________________;
写出该反应的离子方程式
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。某研究性学习小组在实验室中配制1 mol·L-1的稀硫酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是________填字母序号)。
A.实验中所用到的滴定管、容量瓶,在使用前均需要检漏
B.如果实验中需用60 mL的稀硫酸标准溶液,配制时应选用100 mL容量瓶
C.容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小
D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大
E.配制溶液时,定容时俯视读数,则导致实验结果偏大
F.中和滴定结束时俯视读数,则导致实验结果偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
对于常温下pH=3的乙酸溶液,下列说法正确的是双选) )。
A.cH+)=cCH3COO-)+cOH-)
B.加水稀释到原体积的10倍后溶液pH变为4
C.加入少量乙酸钠固体,溶液pH升高
D.与等体积pH为11的NaOH溶液混合后所得溶液中:cNa+)=cCH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
用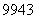 Tc给低产油田作“钡透”,能实现原油的增产增收。下列有关
Tc给低产油田作“钡透”,能实现原油的增产增收。下列有关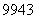 Tc的说法中正确的是双选) )。
Tc的说法中正确的是双选) )。
A.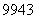 Tc与
Tc与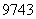 Tc互为同素异形体
Tc互为同素异形体
B.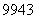 Tc含有43个中子
Tc含有43个中子
C.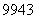 Tc与
Tc与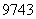 Tc的化学性质相同
Tc的化学性质相同
D.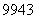 Tc的中子数比电子数多13
Tc的中子数比电子数多13
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的稀盐酸跟过量锌粉反应时,为了加快反应速率又不影响生成H2的总量,可采取的措施是( )
A.加入少量稀氢氧化 钠溶液
钠溶液
B.加入少量CH3COONa固体
C.加入少量NH4HSO4固体
D.加入少量CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.任何油脂在碱性条件下水解都能生成甘油
B.蔗糖水解前后均可发生银镜反应
C.不同的单糖含有的官能团相同
D.向蛋白质中加入CuSO4溶液发生盐析
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com