
绿色化学中,最理想的“原子经济”是原子利用率为100%。下列反应类型能体现“原子经济性”原则的是 ( )
①取代反应 ②加成反应 ③酯化反应 ④水解反应 ⑤加聚反应
A. ②⑤ B. ①② C. ③④ D. ②④
科目:高中化学 来源: 题型:
乙醚极易挥发、微溶于水、是良好的有机溶剂。乙醇与浓硫酸的混合物在不同温度下反应能生成乙烯或乙醚。某实验小组用下图装置制取乙醚和乙烯。
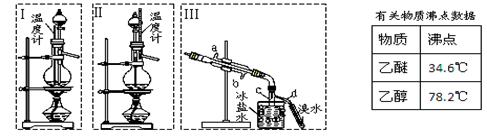
(1)制乙醚:在蒸馏烧瓶中先加入10 mL乙醇,慢慢加入10 mL浓硫酸,冷却,固定装置。加热到140℃时,打开分液漏斗活塞,继续滴加10 mL乙醇,并保持140℃,此时烧瓶
c中收集到无色液体。
①Ⅰ和Ⅱ是反应发生装置,应该选择 (选答“Ⅰ”或“Ⅱ”)与装置Ⅲ相连。
②乙醇通过分液漏斗下端连接的长导管插入到液面下加入,目的有二,一是使反应物充分混合,二是 。
(2)Ⅲ中水冷凝管的进水口是 (选答“a”或“b”)。
冰盐水的作用是
(3)有同学认为以上装置还不够完善,一是溴水可能倒吸,二是尾气弥漫在空气中遇明火
危险。该同学设计了以下几种装置与导管d连接,你认为合理的是(选填编号) 。
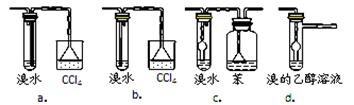
(4)反应一段时间后,升温到170℃,观察到反应物变为黑色,溴水褪色。写出实验过程中生成了酸性气体的化学方程式及其使溴水褪色的化学方程式:
; 。
(5)实验中收集到的乙醚产品中可能含有多种杂质。某同学设计了以下提纯方案:
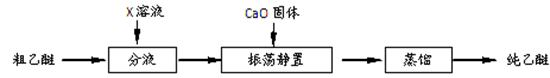
①分液步骤除去产品中的酸性杂质,则X可以是 。
②蒸馏操作可除去的杂质是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质中,化学键的类型相同的是 ( )
A. HCl、MgCl2、NH4Cl B. H2O、Na2O、CO2
C. CaCl2、NaOH、H2O D. NH3、H2O、CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四种金属。将A与B用导线连接起来,浸入电解质溶液中,B为正极。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们的活动性由强到弱的顺序是( )
A.DCAB B.DBAC C. DABC D.BADC
查看答案和解析>>
科目:高中化学 来源: 题型:
为提纯下列物质(括号内为少量杂质),所选用的除杂式试剂和分离方法正确的是( )
| 提纯物质 | 除杂试剂 | 分离法 | |
| A | KCl溶液(FeCl3) | 氨水 | 过滤 |
| B | 乙酸乙酯(乙酸) | 乙醇和浓硫酸 | 分液 |
| C | Fe粉(Al粉) | NaOH溶液 | 过滤 |
| D | 乙醇(H2O) | 金属钠 | 蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与社会、生产、生活密切相关。下列说法正确的是
A.聚氯乙烯塑料制品可用于食品包装
B.“地沟油”禁止食用,但可以用来制肥皂
C.煤经过气化和液化等物理变化可转化为清洁燃料
D.纤维素、油脂、蛋白质均是天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中富含镁,可经过加碱沉淀、过滤、酸溶、结晶及脱水等步骤得到无水氯化镁,
最后电解得到金属镁。
(1)加碱沉淀镁离子时,生成的Mg(OH)2在分散系中处于沉淀溶解平衡,其溶度积常数表达式
Ksp= ▲ 。
(2)MgCl2溶液显酸性,其水解的离子方程式为 ▲ 。
(3)除去MgCl2酸性溶液中少量的FeCl3,可加入的试剂有 ▲
a.MgO b.Mg(OH)2 c.MgCO3 d.MgSO4
(4)若在空气中加热MgCl2·6H2O,可生成Mg(OH)Cl或MgO,写出相关的化学方程式之一
▲ 。
(5)MgCl2·6H2O在干燥的HCl气流中加热可得到无水氯化镁,其原因是 ▲ 。
(6)电解熔融的MgCl2,阳极的电极反应式为: ▲ ;阴极的电极反应式为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关反应速率的说法正确的是 ( )
A.用铁片和稀硫酸反应制氢气时,改用98﹪的硫酸可以加快反应速率
B.100ml 2mol·L-1 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C.SO2的催化氧化反应是一个放热的反应,所以升高温度,反应速率变慢
D.汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率变慢。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com