
【题目】有机物A为烃类化合物,质谱图表明其相对分子质量为70,其相关反应如下图所示,其中B、D、E的结构中均含有2个—CH3,且它们的核磁共振氢谱中均出现4个峰。

请回答:
(1)D的分子式为______________;
(2)Ⅲ的反应类型为______(填字母序号);
a.还原反应 b.加成反应 c.氧化反应 d.消去反应
(3)写出下列反应的化学方程式:
a.反应Ⅰ:________________________________________________;
b.A在催化剂条件下,反应生成高聚物:______________________________;
(4)A分子中最多有_______个原子共平面,A的同分异构体中有一对互为顺反异构的链状有机物,且结构中含有2个—CH3,它们的结构简式为_______和________;
(5)E的一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为_______________。
【答案】 C5H10O a、b (CH3)2CHCH2CH2Br+NaOH![]() (CH3)2CHCH=CH2+NaBr+H2O CH(CH3)2CH=CH2
(CH3)2CHCH=CH2+NaBr+H2O CH(CH3)2CH=CH2![]()
![]() 8
8 ![]()
![]()
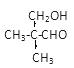
【解析】B可在NaOH乙醇溶液加热的条件下反应生成A,则A中含有C=C,有机物A为烃类化合物,质谱图表明其相对分子质量为70,根据70÷14=5可判断A的分子式为C5H10,B的分子式为C5H11Br,D能与银氨溶液反应,说明D中含有-CHO,E中含有-COOH,B、D、E的结构中均含有2个-CH3,它们的核磁共振氢谱中均出现4个峰,说明含有4种不同的H原子,D应为 (CH3)2CHCH2CHO,E应为 (CH3)2CHCH2COOH,C为 (CH3)2CHCH2CH2OH,B为(CH3)2CHCH2CH2Br,则A为(CH3)2CHCH=CH2。
(1)由以上分析可知D为(CH3)2CHCH2CHO,分子式为C5H10O;(2)反应Ⅲ为加成反应,与氢气加成反应生成醇,也为还原反应,答案选a、b;(3)反应Ⅰ为(CH3)2CHCH2CH2Br在乙醇作用下与NaOH反应生成烯烃,为消去反应,方程式为(CH3)2CHCH2CH2Br+NaOH![]() (CH3)2CHCH=CH2+NaBr+H2O;A含有碳碳双键,发生加聚反应生成高分子化合物,方程式为(CH3)2CHCH=CH2
(CH3)2CHCH=CH2+NaBr+H2O;A含有碳碳双键,发生加聚反应生成高分子化合物,方程式为(CH3)2CHCH=CH2![]()
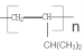 ;(4)A中含有碳碳双键,由于碳碳双键的平面形结构,而碳碳单键可以旋转,所以A分子中最多有8个原子共平面;A有顺反异构且结构中有2个-CH3的A的同分异构体中,C=C上应连接两个不同的烃基,结构简式为
;(4)A中含有碳碳双键,由于碳碳双键的平面形结构,而碳碳单键可以旋转,所以A分子中最多有8个原子共平面;A有顺反异构且结构中有2个-CH3的A的同分异构体中,C=C上应连接两个不同的烃基,结构简式为![]() 或
或![]() ;(5)E有多种同分异构体,其中能发生银镜反应,说明含有-CHO,能与足量金属钠生成氢气,说明含有-OH,不能发生消去反应,说明-OH邻位的C原子上不含H,则可能的结构简式为
;(5)E有多种同分异构体,其中能发生银镜反应,说明含有-CHO,能与足量金属钠生成氢气,说明含有-OH,不能发生消去反应,说明-OH邻位的C原子上不含H,则可能的结构简式为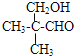 。
。


科目:高中化学 来源: 题型:
【题目】以下关于石油化工的认识不正确的是
A. 塑料、橡胶、纤维都是石油化工的产品
B. 石油裂化的主要目的是为了提高轻质液体燃料的产量
C. 使用合适的催化剂可以提高石蜡裂化的产量
D. 裂化汽油含有不饱和碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(FeSO4·7H2O)是治疗缺铁性贫血的特效药。下面是以商品级纯度铁屑(含少量锡等杂质)生产绿矾的一种方法:

已知:在H2S饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。
(1)检验得到的绿矾晶体中是否含有Fe3+的实验操作是_________。
(2)操作Ⅱ在溶液中用硫酸酸化至pH=2的目的是_________;通入硫化氢至饱和的目的是:①除去操作Ⅰ所得溶液中含有的Sn2+等杂质离子;②_________。
(3)操作Ⅳ的顺序依次为_________、冷却结晶、_________。
(4)操作Ⅳ得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②__________。
(5)测定绿矾产品中Fe2+含量的方法是:a.称取2.850 g绿矾产品,溶解,在250 mL容量瓶中定容;b.量取25.00 mL待测溶液于锥形瓶中;c.用硫酸酸化的0.010 00 mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00 mL(滴定时KMnO4溶液只与Fe2+发生反应)。
①计算上述样品中FeSO4·7H2O的质量分数为_________(保留4位有效数字)。
②若用上述方法测定的样品中FeSO4·7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“重整碳九"是指含有9个碳原子的芳香烃,分子式为C9H12的芳香烃中,含有两个侧链的同分异构体有
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O4是一种无色气体,常被用作火箭推进剂组分中的氧化剂。
(1)已知:①2O2(g)+N2(g)![]() N2O4(l) △H1;
N2O4(l) △H1;
②N2O4 (l)+O2(g)![]() N2(g)+2H2O(g) △H2;
N2(g)+2H2O(g) △H2;
联氨和从N2O4作为火箭推进剂时发生反应:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) 的△H=_________(用含△H1、△H2的式子表示)。
(2)一定温度下,在容积为2L的恒容密闭容器中充入xmolN2O4(g),发生反应:N2O4(g)![]() 2NO2(g) △H=+24.4kJ/mol。体系中NO2浓度随时间变化的情况如图所示。
2NO2(g) △H=+24.4kJ/mol。体系中NO2浓度随时间变化的情况如图所示。

①下列可作为判断反应达到平衡的依据是_______ (填序号)。
a.v正(N2O4)=2v逆(NO2). b.体系颜色不变
c.气体平均相对分子质量不变 d.气体密度不变
② ta时,v正_________v逆(填“>”“ =”或“<”,下同);ta时v逆____________tb时v逆。
③该反应的平衡常数K=__________。
④对于气体参与的反应,平衡常数也可用气体组分(B)的平衡分压p(B)代替该气体的平衡浓度c(B),
则该反应平衡常数KP=_____________ (用表达式表示);已知:上述反应中,正反应速率为v正=k正·p(N2O4),逆反应速率v逆= k逆·p2(NO2),其中k正、k逆为速率常数,则k正为_______________以k逆、KP表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,既能发生水解反应,又能发生加成反应,但不能发生消去反应的是( )
A.CH2=CH—CH2CH2ClB.CH2=CHCH2COOCH3
C.CH3CHClCH=CH2D.(CH3)3CCH2Br
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com