
| A. | 1 mol乙炔分子所含的共用电子对总数为5NA | |
| B. | 1 mol甲基(-CH3 )所含的电子总数为9NA | |
| C. | 0.5 mol 1,3-丁二烯分子中含有碳碳双键总数为NA | |
| D. | 标准状况下,22.4L己烷完全燃烧所生成的气态产物的分子数为7NA |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3溶液中加入铁粉:Fe+Fe3+═2Fe2+ | |
| B. | NH4HSO4溶液中加入少量NaOH:NH4++OH-═NH3•H2O | |
| C. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | 氯气通入Na2SO3溶液中:Cl2+SO32-+H2O═SO42-+2H++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯原子的结构示意图: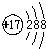 | |
| B. | 硫酸的电离方程式:H2SO4═H2++SO42- | |
| C. | 苏打粉的化学式:NaHCO3 | |
| D. | 明矾的化学式:KAl(SO4)2•12H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气通过灼热的CuO粉末 | B. | 将锌粒投入Cu(NO3)2溶液 | ||
| C. | CO高温下还原Fe2O3 | D. | 二氧化碳通过Na2O2粉末 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液加入几滴KSCN溶液后不变色再滴加几滴氯水后,溶液变红,说明该溶液一定有Fe2+ | |
| B. | 某溶液滴加AgNO3溶液产生白色沉淀,说明该溶液一定含Cl- | |
| C. | 某溶液加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,说明该溶液一定有CO32- | |
| D. | 某溶液滴加盐酸酸化的BaCl2溶液后,有白色沉淀产生,说明该溶液一定含SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
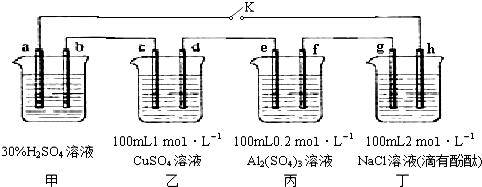
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com