
| A.甲与金属反应时得电子的数目比乙多 |
| B.甲单质的熔沸点比乙的低 |
| C.甲的氧化物对应的水化物酸性比乙强 |
| D.甲能将乙的简单离子从其盐溶液中置换出来 |
科目:高中化学 来源:不详 题型:问答题
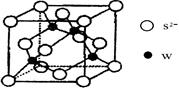
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ⑥ | | ⑦ | ⑨ | |
| 3 | ① | ③ | ⑤ | | | | ⑧ | ⑩ |
| 4 | ② | ④ | | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.Y的最高化合价为+6 |
| B.离子半径:W>Q>Y>X |
| C.氢化物的沸点:Y>Q |
| D.最高价氧化物的水化物的酸性:W>Q |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②④⑤ | B.①②④ | C.②③⑤ | D.全部正确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.1.10 ×10-10 m | B.0.80×10-10 m | C.1.20× 0-10 m | D.0.70×10-10 m |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO + H2S
CO + H2S 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相 关 信 息 |
| A | A的基态原子最外层电子排布式为2s22p3 |
| B | B是地壳中含量最高的元素 |
| C | C+与B的简单离子的电子层结构相同 |
| D | D的一种核素的质量数为64,中子数为35 |
| E 、F | E 、F既同周期又同族,且原子序数F比E多2 |
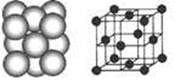
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HClO4、H2SO4、H3PO4的酸性依次增强 |
| B.P、S、Cl最高正价依次升高 |
| C.HCl、HBr、HI的稳定性依次增强 |
| D.锂、钠、钾的金属性依次增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com