
| 配料 | 精制盐、碘酸钾(以I计,18-33mg/kg) |
| 食用方法 | 烹饪时加入,菜熟后最佳 |
| 保存方法 | 密封避光,常温防潮 |
| A、此食盐是混合物 |
| B、“烹饪时加入,菜熟后最佳”的原因可能是碘酸钾受热不稳定 |
| C、碘酸钾(KIO3)中碘的化合价+5 |
| D、1kg此食盐中含碘酸钾(18-33)mg |


科目:高中化学 来源: 题型:
| A、HCO3-+OH-═CO32-+H2O |
| B、2Fe3++Fe═3Fe2+ |
| C、H3PO4+2OH-═HPO4-+2H2O |
| D、Zn+2H+═Zn2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
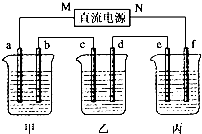 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.查看答案和解析>>
科目:高中化学 来源: 题型:
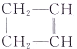 )在一定条件下可被氧化成丁二醛.现有某有机化合物A(C6H8),在一定条件下与足量氢气反应可生成饱和有机化合物B(C6H12).若用某氧化剂来氧化有机化合物A时,生成丙二醛(OHC-CH2-CHO).则:
)在一定条件下可被氧化成丁二醛.现有某有机化合物A(C6H8),在一定条件下与足量氢气反应可生成饱和有机化合物B(C6H12).若用某氧化剂来氧化有机化合物A时,生成丙二醛(OHC-CH2-CHO).则:查看答案和解析>>
科目:高中化学 来源: 题型:
A、2NaCl(熔融)
| ||||
B、MgO+H2
| ||||
C、Fe3O4+4CO
| ||||
D、2HgO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含NA个铜原子的CuO和Cu2S的混合物质量为80.0 g |
| B、标准状况下,22.4 L氧气作氧化剂时转移电子数为4NA |
| C、500 mL、2 mol?L-1碳酸钠溶液中带电粒子数一定大于3NA |
| D、50 mL 18 mol?L-1浓硫酸与足量锌粒反应,产生的气体分子数小于0.9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②⑤⑧ | B、③⑤⑦⑧ |
| C、①⑤⑧ | D、②④⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
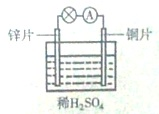 如图所示装置能使反应Zn+H2SO4═ZnSO4+H2↑的氧化反应和还原反应分别在锌片和铜片上进行,所以电流计指针发生了偏转.下列说法不正确的是( )
如图所示装置能使反应Zn+H2SO4═ZnSO4+H2↑的氧化反应和还原反应分别在锌片和铜片上进行,所以电流计指针发生了偏转.下列说法不正确的是( )| A、锌片发生氧化反应 |
| B、铜片上有气体产生 |
| C、电子由铜片通过导线流向锌片 |
| D、铜片上发生反应2H++2e-═H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com