
| A��ת�ƴ���Һ������ƿʱ��δϴ���ձ� |
| B����ʽ�ζ���������ˮϴ�Ӻ�ֱ��װ���� |
| C���ζ�ʱ��Ӧ��ҡ��̫���ң�������Һ�彦�� |
| D���ζ����յ�ʱ���ζ��ܼ����������� |


 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��С�ձ��ڲ�����ˮ����ʹ��õķ�Ӧ����ֵƫС |
| B���ᡢ����ʱ��Ӧ����Ͳ�е���Һ���������ձ�����Һ�У��Է�Һ���⽦ |
| C���ձ���������ֽ���������ǹ̶�С�ձ� |
| D��������ͬŨ�Ⱥ�������������ϡ������Һ����ʵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A������10.00 mL | B����10.00 mL |
| C������10.00 mL | D������11.00 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
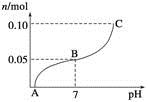
| A��A��ʱpH��1 |
| B��ǡ����ȫ����ʱBa(OH)2�����Ϊ2 L |
C��B��ʱ����Һ�е�����Ũ�ȹ�ϵΪc(Na��)��c(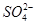 )��c(H��)��c(OH��) )��c(H��)��c(OH��) |
| D��C��ʱpH��14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ԭ�� | ��Ȼ�� | ���� | ú |
| ���Ͷ�ʷ��� | 1.0 | 1.5 | 2.0 |
| ��������/J��t��1 | 28��109 | 38��109 | 48��109 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ | B������ | C������ | D�����ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��a=b="10" mL | B��a=b>10 mL | C��a<b | D��a>b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ú��ʯ�͡���Ȼ����ȼ��������������Դ |
| B��ú��ʯ�͡�ˮú���ɴ���Ȼ��ֱ�ӻ�ȡ,��һ����Դ |
| C��̫������һ����Դ������Դ����������Դ |
| D����ϫ����Դ�������������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com