
25℃时,已知弱酸的电离常数:Ki(CH3COOH) = 1.8 ×10-5;Ki1(H2CO3) = 4.4 ×10-7;Ki2(H2CO3) = 4.7 × 10-11;Ki(HClO) = 4.0 ×10-8。则下列说法正确的是
A.物质的量浓度相等的溶液pH关系:pH(NaClO)>pH(Na2CO3)>pH(CH3COONa)
B.向NaClO溶液中通少量CO2:CO2 + NaClO + H2O → NaHCO3 + HClO
C.a mol/L HClO与b mol/L NaOH溶液等体积混合后所得溶液中c(Na+)>c(ClO-),则a一定小于b
D.向氯水中加入NaHCO3固体,可以增大氯水中次氯酸的浓度
BD
【解析】
试题分析:A、电离常数越大酸性越强,则根据电离常数可知酸性强弱顺序是CH3COOH>H2CO3>HCO3->HclO。酸越弱,相应的钠盐越容易水解,溶液碱性越强,则物质的量浓度相等的溶液pH关系:pH(Na2CO3)>pH(NaClO)>pH(CH3COONa),A错误;B、向NaClO溶液中通少量CO2生成碳酸氢钠和次氯酸,即CO2 + NaClO + H2O → NaHCO3 + HclO,B正确;C、a mol/L HClO与b mol/L NaOH溶液等体积混合后所得溶液中c(Na+)>c(ClO-),则根据电荷守恒可知溶液显碱性,二者如果恰好反应生成的次氯酸钠水解溶液也显碱性,因此a不一定小于b,C错误;D、向氯水中加入NaHCO3固体,碳酸氢钠与盐酸反应,但与次氯酸不反应,促进氯气的溶解,因此可以增大氯水中次氯酸的浓度,D正确,答案选BD。
考点:考查电离常数的应用


 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源:2014-2015黑龙江省绥化市三校高一上学期期末联考化学试卷(解析版) 题型:选择题
下列物质不能通过化合反应直接制得的是
A.FeCl2 B.NaHCO3 C.Al(OH)3 D.Fe3O4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省攀枝花市高三上学期第二次统考理综化学试卷(解析版) 题型:实验题
(14分)为了探究二氧化硫的漂白作用到底是二氧化硫本身还是二氧化硫与水作用的产物,某学习小组设计了如图装置来进行实验。

请回答下列问题:
(1)亚硫酸钠与浓硫酸反应的化学方程式是 。
为了探究干燥的SO2 能不能使品红褪色,请指出设计的实验装置图中两个明显的不足:① ;② 。
(2)按照修改后的装置,实验中控制SO2以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色。这说明品红褪色的原因不是SO2直接导致。为此,SO2 通过品红水溶液后,引起品红褪色的微粒可能是 。
(3)甲同学实验如下:取等量、相同浓度的品红水溶液于两支试管中,再分别加入少量亚硫酸钠固体和亚硫酸氢钠固体,两支试管中的品红都褪色,对此,他得出结论:使品红褪色的微粒是HSO3-、SO32- ,不是H2SO3。乙同学认为他的结论不正确, 其理由是 。
(4)为了进一步探究,乙组同学做了如下实验:分别取相同浓度的品红溶液各20mL加入两只小烧杯中,两只烧杯中同时一次性各加入20mL0.1mol/L的亚硫酸钠溶液和20mL0.1mol/L的亚硫酸氢钠溶液,发现加入亚硫酸钠溶液的品红褪色明显较快。小组同学分别比较了两种溶液中各微粒浓度与褪色快慢的关系,得出的结论是 ,理由是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省达州市普高高三上学期第一次诊断理综化学试卷(解析版) 题型:选择题
下列有关说法不正确的是
A.SO42-的空间构型是正四面体形
B.CS2分子中各原子均达8电子稳定结构
C.CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
D.H2O2分子是既含极性键又含非极性键的非极性分子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闸北区高三上学期期末化学试卷(解析版) 题型:填空题
(本题共12分)葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→ (C6H11O7)2 Ca (葡萄糖酸钙)+H2O+CO2
相关物质的溶解性见下表:
物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
实验流程如下:
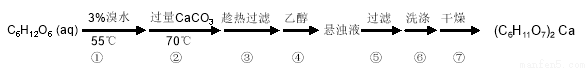
请回答下列问题:
32.第②步中所加CaCO3还发生了其他反应,写出其中一个主要反应的方程式________;充分反应后CaCO3固体需有剩余,目的是______________________;
33.第③步需趁热过滤,原因是______________________;
34.第④步加入乙醇的作用是______________________;
35.第⑥步中,下列洗涤剂最合适的是________。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
锌是人体健康所必需的元素,葡萄糖酸锌是一种常用的补锌剂,对婴儿及青少年的智力和身体发育有重要作用。工业上以葡萄糖酸钙为原料通过如下两步制备葡萄糖酸锌:
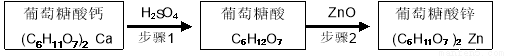
步骤1:充分反应后,过滤除去CaSO4沉淀。步骤2:将葡萄糖酸溶液与ZnO混合。
36.步骤2中,待其充分反应后,须继续加入葡萄糖酸溶液至pH为5.8,目的是 。
37.下列物质可替代ZnO的是 (填字母)。
a.NH3·H2O
b.Zn(OH)2
c.NaOH
d.ZnSO4
e.ZnCO3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闸北区高三上学期期末化学试卷(解析版) 题型:选择题
元素周期表中短周期的一部分如图,关于X、Y、Z、W、Q说法正确的是
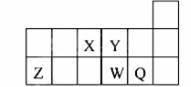
A.元素Y与元素Z的最高正化合价之和的数值等于9
B.原子半径的大小顺序为:W>Z>Y
C.离子半径的大小顺序为:W2->Y2->Z3+
D.W的气态氢化物的热稳定性和还原性均比Q强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:选择题
H2C2O4是一种二元弱酸,NaHC2O4溶液显酸性。现测得某溶液中存在的离子有C2O42-、HC2O4-、OH-、Na+、H+。下列判断正确的是
A.该溶液的溶质只能是Na2C2O4或NaHC2O4或两者的混合物
B.该溶液可能显酸性、碱性或中性
C.溶液中一定存在c(Na+) > c(HC2O4- )
D.溶液中一定存在c(H+) - c(OH-) > c(HC2O4- ) - c(Na+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市嘉定区高三一模化学试卷(解析版) 题型:选择题
下列各图中,纵坐标表示能量,横坐标表示反应过程,均从反应物开始。则表示在催化剂作用下,正反应是吸热反应的,比较合理的图象是
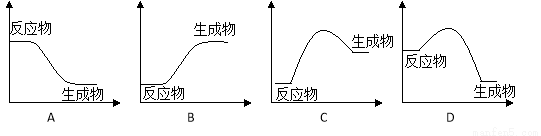
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com