
| 化学键 | 断开1mol化学键所需的能量(kJ) |
| H-H | 436 |
| O-H | 463 |
| O=O | 498 |
 .
.| 实验编号 | 反应物 | 催化剂 | |
| a | 50mL 5% H2O2溶液 | 1mL 0.1mol•L-1 FeCl3溶液 | |
| b | 50mL 5% H2O2溶液 | 少量浓盐酸 | 1mL 0.1mol•L-1 FeCl3溶液 |
| c | 50mL 5% H2O2溶液 | 少量浓NaOH溶液 | 1mL 0.1mol•L-1 FeCl3溶液 |
| d | 50mL 5% H2O2溶液 | MnO2 | |
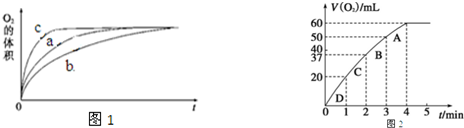
分析 (1)①水为共价化合物,水中O原子核外为8个电子;
②水分解生成氧气和氢气,根据共价键断裂吸收能量,形成化学键放出能力,结合方程式计算反应热;
③11.2L(标准状况)的H2为0.5mol,可生成0.5mol水,以此解答;
(2)①溶液的酸碱性不同,反应的速率不同;
②由图象可知,曲线斜率逐渐减小,说明反应速率逐渐减小,结合浓度对反应速率的影响解答该题;根据方程式计算过氧化氢浓度.
解答 解:(1)①H2O是共价化合物,是由原子和氢原子形成共价键,电子式为 ,
,
故答案为: ;
;
②水分解生成氧气和氢气,方程式为2H2O=2H2+O2,可知2molH2O(g)分解,生成2mol氢气和1mol氧气,则断裂4molO-H,形成1molO=O键、2mol H-H键,
所以吸收的热量为4mol×463kJ/mol=1852kJ,
放出的热量为498kJ+2×436kJ=1370kJ,
所以吸收的热量为1852kJ-1370kJ=482kJ,
所以热化学方程式为2H2O(g)=2H2(g)+O2(g)△H=+482KJ/mol,
故答案为:2H2O(g)=2H2(g)+O2(g)△H=+482KJ/mol;
③11.2L(标准状况)的H2为0.5mol,可生成0.5mol水,生成气态水放出的热量为0.5mol×$\frac{1}{2}$×482KJ=120.5kJ,
故答案为:120.5;
(2)①abc溶液的酸碱性不同,反应的速率不同,由图象可知在碱性条件下反应速率最大,在酸性条件下反应速率最小,可以得出的结论是其它条件不变,碱性环境能加快H2O2的分解速率,酸性环境能减缓H2O2的分解速率,
故答案为:其他条件不变时,在碱性环境下加快H2O2的分解速率,酸性环境下减缓H2O2的分解速率;
②由图象可知,曲线斜率逐渐减小,说明反应速率逐渐减小,原因是反应物的浓度逐渐减小的原因,
由反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应为不可逆反应,在5min后,收集到的气体体积不再增加,说明过氧化氢完全分解,
由图象可知,生成氧气的体积为60mL,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
2mol 22.4L
n(H2O2) 0.06L
n(H2O2)=$\frac{2mol×0.06L}{22.4L}$=0.00536mol,所以c(H2O2)=$\frac{0.00536mol}{0.05L}$=0.11 mol•L-1,
故答案为:随着反应的进行,H2O2的浓度逐渐减小,H2O2的分解速率逐渐减慢;0.11 mol•L-1.
点评 本题考查较为综合,涉及化学反应与能量变化,热化学方程式的书写、反应热的计算,化学反应速率的探究等知识,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意相关基础知识的积累,难度中等.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源:2016-2017学年湖南省高一上第一次月考化学试卷(解析版) 题型:选择题
关于粗盐提纯的下列说法中正确的是( )
A.溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解
B.滤去不溶性杂质后,将滤液移至坩埚内加热浓缩
C.当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干
D.将制得晶体转移到新制过滤器中用大量水进行洗涤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
恒容容器中,2SO2(g) + O2(g) 2SO3 (g) △H=-296.6kJ/mol,下列判断不正确的是
2SO3 (g) △H=-296.6kJ/mol,下列判断不正确的是
A.2体积SO2和足量O2反应,一定不能生成2体积SO3
B.其他条件不变,增大压强,正反应速率增大逆反应速率也增大
C.加入2molSO2和1molO2放出的热量是加入1molSO2和0.5molO2放出热量的2倍
D.平衡后再加入1molSO3,SO2的转化率增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高二上第一次月考化学卷(解析版) 题型:选择题
能证明Na2SO3溶液中存在SO32-+H2O  HSO3-+OH-水解平衡事实的是
HSO3-+OH-水解平衡事实的是
A.滴入酚酞溶液变红,再加入H2SO4溶液后红色退去
B.滴入酚酞溶液变红,再加入氯水后红色退去
C.滴入酚酞溶液变红,再加入NaOH溶液后红色加深
D.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色退去
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高二上第一次月考化学卷(解析版) 题型:选择题
下列有关实验的说法正确的是
A. 用湿润的pH试纸测稀盐酸的pH
B. 用酸式滴定管量取20.00 mL酸性K2Cr2O7溶液
C. 用托盘天平称取5.85 gNaCl晶钵
D. 用带磨口玻璃塞的试剂瓶保存Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol CO2和1 mol CO所占的体积相同,所含分子数相同 | |
| B. | 1 g CO和1 g CO2所占的体积不同,所含分子数不同 | |
| C. | 在任何情况下,1 mol CO2和64 g SO2所含有分子数和原子总数都相同 | |
| D. | 某物质若含阿伏加德罗常数个微粒,该物质标准状况下体积约为22.4 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com