
| A.用水鉴别乙醇、甲苯和溴苯 |
| B.用燃烧法鉴别乙醇、苯和四氯化碳 |
| C.用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 |
| D.用酸性高锰酸钾溶液鉴别苯、环已烯和环已烷 |
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源:不详 题型:实验题
| A.澄清石灰水,浓H2SO4 | B.酸性KMnO4,浓H2SO4 |
| C.溴水,浓H2SO4 | D.浓H2SO4,溴水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

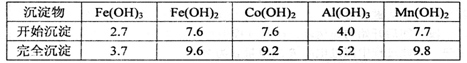

| A.2.0~2.5 | B.3.0~3.5 | C.4.0~4.5 | D.5.0~5.5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 序号 | 物质 | 除杂试剂 |
| (1) | CO2(HCl) | |
| (2) | Fe2O3(Al2O3) | |
| (3) | NaCl溶液(MgCl2) | |
| (4) | NO气体(NO2) | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
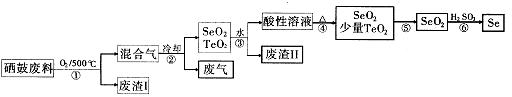
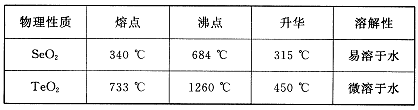
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
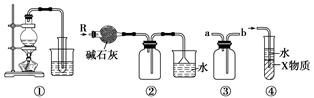
| A.装置①可制取少量蒸馏水 |
| B.装置②可用于干燥、收集氨气,并吸收多余的氨气 |
| C.装置③可用于排空气法收集H2、CO2、Cl2、HCl、NO等气体 |
| D.装置④中X物质若为四氯化碳,则可用于吸收氨气或氯化氢 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验操作 | 现象 | 解释或结论 |
| A | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X中一定含有SO |
| B | 等体积pH=3的HA和HB 两种酸分别与足量的锌反 应,排水法收集气体 | HA放出的氢气多且反应速率快 | HB酸性比HA强 |
| C | 在镁、铝为电极,氢氧化钠为电解质的原电池装置中 | 镁表面有气泡 | 金属活动性:Al>Mg |
| D | 向1 mL 1%的NaOH溶液中 加入2 mL 2%的CuSO4溶 液,振荡后加入0.5 mL有 机物Y,加热 | 未出现砖红色 沉淀 | Y中不含有醛基 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
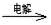 MnO2+Zn+2H2SO4。
MnO2+Zn+2H2SO4。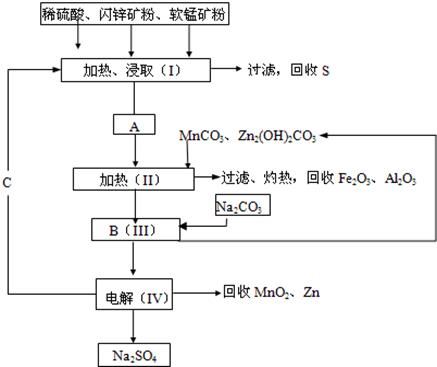
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | A | B | C | D |
| 装置 | 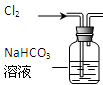 | 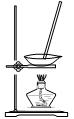 | 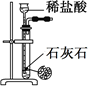 |  |
| 目的 | 除去Cl2中含有的少量HCl | 蒸干NH4Cl饱和溶液制备NH4Cl晶体 | 制取少量纯净的CO2气体 | 分离CCl4萃取碘水后已分层的有机层和水层 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com