
| A、2.24L H2O(标况) |
| B、22g CO2 |
| C、9.03×1023个O2 |
| D、2mol H2 |
| m |
| M |
| N |
| NA |
| m |
| M |
| 2.24×103g |
| 18g/mol |
| 22g |
| 44g/mol |
| N |
| NA |
| 9.03×1023 |
| 6.02×1023 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、标准状况下,22.4LNH3和CH4的混合气体,所含分子数为NA |
| B、常温常压下,28gCO中所含碳原子数为 NA |
| C、1 L 0.5mol?L-1的MgCl2溶液中,含有Cl-的个数为NA |
| D、1molCl2与铁反应转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、非金属性:Y>Z>M |
| B、离子半径:M->Z2->Y- |
| C、ZM2分子中各原子的最外层均满足8电子稳定结构 |
| D、三种元素中,Y的最高价氧化物对应的水化物酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
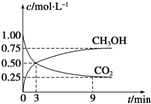 ①CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)浓度随时间变化如图2所示.从3min到9min,v(H2)=
①CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)浓度随时间变化如图2所示.从3min到9min,v(H2)=| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.13 mol |
| B、1 mol |
| C、1.05 mol |
| D、0.05 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、Ⅰ图中:若MnO2过量,则浓盐酸可全部消耗完 |
| B、Ⅰ图中:不能将导管伸入液面以下,会产生倒吸现象 |
| C、Ⅱ图中:量筒中气体颜色变浅,液面上升,发生了取代反应 |
| D、Ⅲ图中:铜在氯气中燃烧生成蓝色的烟 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com