
| A、热稳定性:HF>H2O>NH3 | B、酸性:HClO4>H2SO4>H3PO4 | C、原子半径:Na>Si>F>H | D、沸点:F2>Cl2>Br2>I2 |


科目:高中化学 来源:物理教研室 题型:021
下列关于物质性质递变规律的叙述中不正确的是
[ ]
A.原子的还原性:K>Na>Mg>Al
B.原子的氧化性:F>Cl>S>P
C.含氧酸的酸性: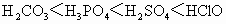
D.氢化物稳定性: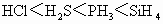
查看答案和解析>>
科目:高中化学 来源: 题型:021
下列关于物质性质递变规律的叙述中不正确的是
[ ]
A.原子的还原性:K>Na>Mg>Al
B.原子的氧化性:F>Cl>S>P
C.含氧酸的酸性: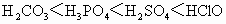
D.氢化物稳定性: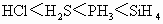
查看答案和解析>>
科目:高中化学 来源:广东省2009届高三化学各地名校月考试题汇编-碳硅及其化合物 题型:021
|
下列关于物质性质的叙述中,正确的是: | |
A. |
浓硫酸具有吸水性,能使胆矾晶体由蓝变白 |
B. |
同温同物质的量浓度的Na2CO3溶液和NaHCO3溶液,后者的碱性弱 |
C. |
过量铁粉加入CuCl2溶液中,充分反应后溶液中的阳离子主要是Fe3+ |
D. |
硅是应用广泛的半导体材料,常温下易与氧气、氯气、硫酸等物质反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质性质的叙述中,正确的是
A.浓硫酸具有吸水性,能使胆矾晶体由蓝变白
B.同温同物质的量浓度的Na2CO3溶液和NaHCO3溶液,前者的碱性弱
C.过量铁粉加入CuCl2溶液中,充分反应后溶液中的阳离子主要是Fe3+
D.硅是应用广泛的半导体材料,常温下易与氧气、氯气、硫酸等物质反应
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com