
【题目】元素X位于第4周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y基态原子的3p轨道上有1对成对电子。X与Y形成的化合物的晶胞结构如图所示,下列关于该晶体的说法正确的是( )
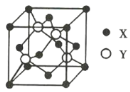
A.该晶体属于原子晶体
B.X2+的配位数为8,Y2-的配位数为4
C.与每个Y2-距离最近且相等的Y2-共有12个
D.该晶体的熔点比氧化锌高
【答案】C
【解析】
元素X位于第四周期,其基态原子的内层轨道全部排满电子,则内层电子数=2+8+18=28,且最外层电子数为2,所以该原子有30个电子,为Zn元素;元素Y基态原子的p轨道上有1对成对电子,说明3p轨道上有4个电子,核外电子排布为1s22s22p63s23p4,则Y是S元素,则化学式为ZnS,据此解题。
A.ZnS含有Zn2+和S2-,属离子晶体,故A错误;
B.因为化学式为ZnS,所以Y2-离子的配位数为4,则X2+离子的配位数也为4,故B错误;
C.由晶胞可知,与每个X2+距离最近的X2+在其面心,则共有![]() =12个,故C正确,
=12个,故C正确,
D.离子晶体ZnO的晶格能比ZnS大,则ZnO的熔点比ZnS高,故D错误;
故答案为C。


科目:高中化学 来源: 题型:
【题目】如图流程中a、b、c、d、e、f是六种有机物,其中a是烃类,其余是烃的衍生物。下列有关说法正确的是( )

A.若a的相对分子质量是42,则d是乙醛
B.若d的相对分子质量是44,则a是乙炔
C.若a为苯乙烯(C6H5—CH=CH2),则f的分子式是C16H32O2
D.若a为单烯烃,则d与f的最简式一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机化合物相关的说法正确的是![]()
![]()
A.糖类、油脂、蛋白质都能水解,但水解产物不同
B.四苯基乙烯![]()

![]() 中所有碳原子一定处于同一平面
中所有碳原子一定处于同一平面
C.![]() 在一定条件下与足量H2反应消耗4mol H2
在一定条件下与足量H2反应消耗4mol H2
D.分子式为C7H8的芳香烃与H2完全加成所得产物的一氯代物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将符合反应类型的反应的序号填在下列分类方法后的横线上
A.4Fe3O4+O2![]() 6Fe2O3
6Fe2O3
B.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
C.Zn+H2SO4=ZnSO4+H2↑
D.CaCO3+2HCl=CaCl2+H2O +CO2↑
E.CH4+2O2![]() CO2+2H2O
CO2+2H2O
F. 3O2![]() 2O3
2O3
G.CuO+H2![]() Cu+H2O
Cu+H2O
H.H2SO4+2NaOH=Na2SO4+2H2O
①属于化合反应的是____(填字母,下同)
②属于分解反应的是____;
③属于复分解反应的是____;
④属于置换反应的是____;
⑤既不属于四种基本反应类型又不属于氧化还原反应的是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H、C、N、O、V(钒)五种元素形成的某分子结构如图所示,下列说法错误是

A.N原子核外存在3种不同能量的电子
B.基态V原子的价电子轨道表示式为![]()
C.基态O原子,电子占据的最高能级符号为2p
D.基态C、N两种原子中,核外存在相同对数自旋方向相反的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上电解NaHSO4溶液制备Na2S2O8。电解时,阴极材料为Pb;阳极(铂电极)电极反应式为2HSO4-- 2e-=S2O82-+2H+。下列说法正确的是( )
A. 阴极电极反应式为Pb+HSO4-- 2e-=PbSO4+H+
B. 阳极反应中S的化合价升高
C. S2O82-中既存在非极性键又存在极性键
D. 可以用铜电极作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是原子半径最大的短周期主族元素,D单质燃烧时呈现黄色火焰,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的离子化合物DF是常用的调味品。试根据以上叙述回答:
(1)元素名称:
A________、B________、C________、D________。
(2)E在元素周期表中的位置:_________________________________________________。
(3)F离子结构示意图:_____________________________________________________。
(4)A、B组成的最简单化合物的名称是____________________________________________。
(5)C、D按原子个数比1∶1组成的一种化合物与水发生反应的化学方程式为___________________________________________________________。
(6)能说明E的非金属性比F的非金属性____(填“强”或“弱”)的事实是________(举一例)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。
①在提纯时为了除去Fe2+,常加入合适的氧化剂,使Fe2+转化为Fe3+,下列物质可作氧化剂的是__(填字母)。
A.KMnO4 B.H2O2 C.氯水 D.HNO3
②然后再加入适当物质调整溶液pH至4,使Fe3+转化为Fe(OH)3,调整溶液pH可选用___(填字母)。
A.NaOH B.NH3·H2O C.CuO D.Cu(OH)2
(2)甲同学怀疑调整溶液pH至4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=1.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常残留在溶液中的离子浓度小于1.0×10-5mol·L-1时就被认定为沉淀完全,设溶液中CuSO4的浓度为3.0mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为__,Fe3+完全沉淀[即c(Fe3+)≤1.0×10-5mol·L-1]时溶液的pH为__,通过计算确定上述方案__(填“可行”或“不可行”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H 是合成抗炎药洛萦洛芬钠的关键中间体,它的一种合成路线如下:

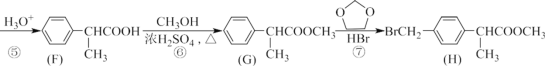
(1)A 的物质名称为_________,H 中非含氧官能团名称是_________。
(2)E 的结构简式为_________,反应⑥的反应类型为_________。
(3)应①的化学方程式为_________,反应⑥的化学方程式为_________。
(4)写出满足下列条件的 F 的同分异构体的结构简式_________。
I.能发生水解反应生成酸和醇
Ⅱ.能发生银镜反应
Ⅲ.核磁共振氢谱有 5 组峰且峰面积之比为 3:2:2:2:1
(5)仿照H 的合成线,设计一种由![]() 合成
合成![]() 的合成路线________。
的合成路线________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com