
【题目】有关下图装置的叙述正确的是

A. 溶液中Na+向Fe极移动
B. 该装置中Pt为正极,电极反应为:O2 + 2H2O + 4e===4OH
C. 该装置中Fe为负极,电极反应为:Fe2e===Fe2+
D. 该原电池装置最终的产物是Fe(OH)2
科目:高中化学 来源: 题型:
【题目】常温下向100mLFeCl3溶液中通入0.224L H2S,生成单质硫,再加入过量铁粉,反应停止后溶液中含有0.06mol阳离子。原FeCl3溶液的物质的量浓度是
A. 0.2 mol/L B. 0.3 mol/L C. 0.4 mol/L D. 0.6 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用下列装置探究Na与CO2反应的还原产物,已知PdCl2+CO+H2O==Pd(黑色)↓+CO2+2HCl。下列相关分析错误的是
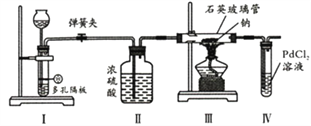
A. I中发生反应可以是Na2CO3+H2SO4==Na2SO4+H2O+CO2↑
B. II中浓硫酸的目的是干燥CO2
C. 实验时,III中石英玻璃管容易受到腐蚀
D. 步骤IV的目的是证明还原产物是否有CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法正确的是
A. 16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1 NA
B. 92.0 g甘油(丙三醇)中含有羟基数为1.0NA
C. 22.4 L(标准状况)氩气含有的质子数为18NA
D. 1.0 mol CH4与Cl2在光照下反应生成的CH3Cl分子数为1.0NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验报告中有以下实验数据,其中数据合理的是( )
A.500 mL容量瓶配制250 mL 0.1mol/L NaCl溶液
B.用量筒量取5.26 mL盐酸
C.用广泛pH试纸测得溶液的pH是3.5
D.用25 mL滴定管量出15.80 mL的NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知M为红色金属单质、E为用量最大的的金属,X、Y、Z为含有E元素的化合物。根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):

(1)M和热空气以及稀H2SO4反应的离子方程式_____________________________。
(2)实验室中X溶液的保存方法___________________________________。
(3)鉴别Y溶液的阳离子的常见方法_______________________________。
(4)Cl2将Z氧化为K2EO4的化学方程式___________________________________。
(5)某同学取X的溶液,酸化后加入KI、淀粉溶液,充分振荡后溶液变为蓝色。描述出现蓝色可能的原因_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定气体摩尔体积的实验中,以下情况不影响测定结果的是( )
A.镁条表面的氧化膜未完全擦去B.镁带中含有不与酸反应的杂质
C.反应后没有用注射器抽气D.硫酸过量,镁全部反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应体系中的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
(1)请将Au2O3之外的反应物与生成物分别填入以下空格内:________
![]()
![]()
(2)反应中,被还原的元素是______________,还原剂是___________。
(3)请将反应物的化学式配平后的系数填入下列相应的位置中,并标出电子转移的方向和数目。________
![]()
(4)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂的物质的量之比为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表中的一部分。

根据A—J在周期表中的位置,用元素符号、化学式或反应式回答下列问题:
(1)氧化性最强的单质是___,用一个化学反应证明H单质的氧化性强于G单质__________。
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为_________。
(3)B、C、G、H离子半径由大到小的顺序是_________。
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为______。若以氢氧化钾溶液为电解质溶液时,电池的总反应式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com