
| 过程Ⅳ:B溶液中含有的离子 | 过程Ⅵ:B溶液中含有的离子 | |
| 甲 | 有Fe3+,无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+、又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+、无Fe2+ | 有Fe2+ |
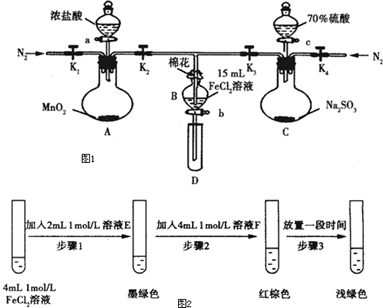
分析 (1)空气中氧气具有氧化性,能干扰实验;
(2)氯气、二氧化硫都有毒,不能直接排空,且氯气、二氧化硫都能和NaOH溶液反应生成无毒物质,可以用碱液吸收;
(3)加热条件下,浓盐酸和二氧化锰反应生成氯化锰、氯气和水;
(4)溶液中氢离子浓度越大反应速率越快;
(5)溶液显酸性,检验SO42-应选择BaCl2溶液;乙中第一次,说明Cl2不足,Cl2氧化性大于Fe3+,第二次有SO42-,说明发生SO2与Fe3+的反应,则氧化性Fe3+>SO2;丙中第一次有Fe3+,无Fe2+,则氧化性Cl2>Fe3+,第二次有Fe2+,说明发生SO2与Fe3+的反应,则氧化性Fe3+>SO2;
(6)增大反应物浓度平衡向正反应方向移动,减小反应物浓度,平衡逆向移动,根据混合物颜色变化判断.
解答 解:(1)空气中氧气具有氧化性,能氧化亚铁离子生成铁离子而干扰实验,为排除氧气的干扰,用氮气将装置中的空气排出,故答案为:排出装置中的空气,防止干扰实验;
(2)氯气、二氧化硫都有毒,不能直接排空,氯气和水反应生成酸、二氧化硫属于酸性氧化物,所以氯气、二氧化硫都能和NaOH溶液反应生成无毒物质,可以用碱液吸收,则棉花浸润的液体是NaOH溶液,
故答案为:NaOH溶液;
(3)加热条件下,浓盐酸和二氧化锰反应生成氯化锰、氯气和水,反应方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(4)溶液中氢离子浓度越大反应速率越快,98%浓硫酸中氢离子浓度小于70%硫酸,所以70%硫酸反应速率较快,故答案为:70%硫酸中氢离子浓度大于98%的硫酸,因此反应速率更快;
(5)溶液显酸性,检验SO42-应选择BaCl2溶液;乙中第一次,说明Cl2不足,Cl2氧化性大于Fe3+,第二次有SO42-,说明发生SO2与Fe3+的反应,则氧化性Fe3+>SO2;丙中第一次有Fe3+,无Fe2+,则氧化性Cl2>Fe3+,第二次有Fe2+,说明发生SO2与Fe3+的反应,则氧化性Fe3+>SO2,
故答案为:乙、丙;
(6)①根据已知条件:FeCl3与SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色,所以可以借助氯化铁和亚硫酸钠溶液来确定假设是否成立,故答案为:Na2SO3;FeCl3;
②根据化学平衡:Fe2+(aq)+SO32-(aq)?FeSO3(s)(墨绿色),步骤3中,Fe3+消耗SO32-,c(SO32-)减小,平衡逆向移动,溶液颜色由红棕色变为浅绿色,
故答案为:Fe3+消耗SO32-,c(SO32-)减小,平衡Fe2+(aq)+SO32-(aq)?FeSO3(s)(墨绿色)逆向移动,溶液颜色由红棕色变为浅绿色.
点评 本题考查性质实验方案设计,为高频考点,涉及实验基本操作过程、化学平衡移动原理、物质的制备、化学反应速率影响因素等知识点,明确实验原理是解本题关键,注意氧化性强弱比较是解答难点,注意(4)题氢离子浓度影响反应速率,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 1/22.4mol/L | B. | V/33.6mol/L | C. | V/22.4mol/L | D. | 1/33.6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0 mol/L的CH3COOH溶液:K+、Fe3+、NO3-、Cl- | |
| B. | l.0 mol•L-1 NaClO溶液:Fe2+、K+、I-、Cl- | |
| C. | 甲基橙显黄色的溶液:Na+、CO32-、NO3-、SO32- | |
| D. | 在c(OH-)/c(H+)=1×1013的溶液:NH4+、Ca2+、C1-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验操作 | 实验现象 | 实验结论 |
| ① | 将镁条投入5mL蒸馏水 | 微量气泡 | Mg与蒸馏水缓慢反应 |
| ② | 将镁条投入5mL饱和NaHCO3溶液中 | 镁表面出现大量气泡 | Mg与NaHCO3溶液剧烈反应 |
| ③ | 将镁条投入5mLNaOH溶液中 | 现象不明显 | Mg与NaOH溶液较难反应 |
| 实验步骤 | 想象和结论 |
| 大试管中加入擦去氧化膜的镁条 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④⑥ | C. | ②③④ | D. | ①③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳 | B. | 石英 | C. | 锗 | D. | 硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0 mol | B. | 1.5 mol | C. | 2.0 mol | D. | 2.5 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com