
| V |
| Vm |
| m |
| n |
| 2.8L |
| 22.4L/mol |
| 2g |
| 0.125mol |
| 16×25% |
| 1 |
| 16-1×4 |
| 12 |
 ,将共用电子对换成短线甲烷结构式,则甲烷的结构式为:
,将共用电子对换成短线甲烷结构式,则甲烷的结构式为: ,甲烷为正四面体结构,
,甲烷为正四面体结构, ;
; ;正四面体结构.
;正四面体结构.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | 氨气 | 硫酸 | 小苏打 | 氧化钙 | 干冰 |
| B | 苛性钠 | 盐酸 | 食盐 | 氧化钠 | 一氧化碳 |
| C | 石灰水 | 冰醋酸(CH3COOH) | 胆矾 CuSO4?5H2O | 过氧化钠 | 二氧化硫 |
| D | 苛性钠 | HNO3 | 碳酸钙 | 氧化铁 | SO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
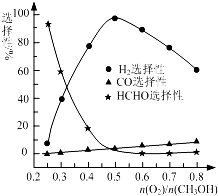 甲醇来源丰富、价格低廉、运输贮存方便,有着重要的用途和应用前景.
甲醇来源丰富、价格低廉、运输贮存方便,有着重要的用途和应用前景.| 1 |
| 2 |
| 1 |
| 2 |
| n(O2) |
| n(CH3OH) |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如下:
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如下: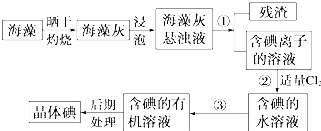
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ksp只与难溶电解质本身的性质和温度有关 |
| B、在一定温度下的AgCl饱和溶液中,C(Ag+)和C(Cl-)的乘积是一个常数 |
| C、在一定温度下,向AgCl饱和溶液中加入盐酸时,Ksp值变大 |
| D、由于Ksp(FeS)>Ksp(CuS),所以FeS沉淀在一定条件下可以转化为CuS沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 X、Y、Z、W有如图所示的转化关系,则X、Y、Z可能是
X、Y、Z、W有如图所示的转化关系,则X、Y、Z可能是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.0×10-7 mol?L-1 |
| B、2.8×10-4 mol?L-1 |
| C、5.6×10-4 mol?L-1 |
| D、7.0×10-5 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生成白色沉淀,加氨水后沉淀溶解,反应前后Ag+的浓度不变 |
| B、生成白色沉淀,加入氨水后沉淀转化成AgOH |
| C、生成白色沉淀,加入氨水后生成了更难溶的配合物Ag(NH3)2Cl? |
| D、向AgNO3溶液中直接滴加氨水,产生的现象与上述相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、依次加入过量硝酸钡和碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸 |
| B、依次加入过量碳酸钾和硝酸钡溶液,过滤,出去沉淀,溶液中补加适量硝酸 |
| C、依次加入过量硝酸钡和碳酸钾溶液,溶液中补加适量硝酸 |
| D、加入过量碳酸钾溶液,过滤,出去沉淀,溶液中补加适量硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com