
 +n HOCH2CH2OH$\stackrel{一定条件}{→}$
+n HOCH2CH2OH$\stackrel{一定条件}{→}$ +(2n-1)H2O.
+(2n-1)H2O. .
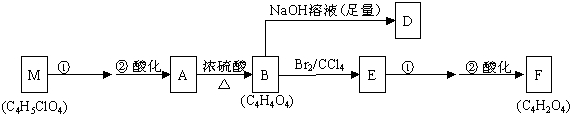
. 分析 A分子式为C4H6O5,不饱和度为$\frac{2×4+2-6}{2}$=2,A与醇(ROH)或羧酸(RCOOH)在浓H2SO4和加热条件下均可反应生成有香味的产物,则A含有羟基、羧基,1mol A与足量的金属钠反应产生1.5mol H2,结合A的电离平衡常数,可知A为二元弱酸,则A分子中含有一个羟基和二个羧基,核磁共振氢谱表明A分子中有5种不同化学环境的氢原子,则A的结构简式为:HOOCCH(OH)CH2COOH,M在氢氧化钠水溶液、加热条件下发生水解反应得到A,故M为HOOCCH(Cl)CH2COOH,A发生消去反应生成B为HOOCCH=CHCOOH,B与足量的NaOH反应生成D为NaOOCCH=CHCOONa,B与溴发生加成反应生成E为HOOCCH(Br)CH(Br)COOH,E在氢氧化钠醇溶液、加热条件下发生消去反应生成,再酸化得到F为HOOCC≡CCOOH,据此解答.
解答 解:A分子式为C4H6O5,不饱和度为$\frac{2×4+2-6}{2}$=2,A与醇(ROH)或羧酸(RCOOH)在浓H2SO4和加热条件下均可反应生成有香味的产物,则A含有羟基、羧基,1mol A与足量的金属钠反应产生1.5mol H2,结合A的电离平衡常数,可知A为二元弱酸,则A分子中含有一个羟基和二个羧基,核磁共振氢谱表明A分子中有5种不同化学环境的氢原子,则A的结构简式为:HOOCCH(OH)CH2COOH,M在氢氧化钠水溶液、加热条件下发生水解反应得到A,故M为HOOCCH(Cl)CH2COOH,A发生消去反应生成B为HOOCCH=CHCOOH,B与足量的NaOH反应生成D为NaOOCCH=CHCOONa,B与溴发生加成反应生成E为HOOCCH(Br)CH(Br)COOH,E在氢氧化钠醇溶液、加热条件下发生消去反应生成,再酸化得到F为HOOCC≡CCOOH.
(1)由上述分析可知,根据化合物A的性质,A分子中含有一个羟基和二个羧基,故选:(b)(c);
(2)由于上述分析可知,A为HOOCCH(OH)CH2COOH,D为NaOOCCH=CHCOONa,F为HOOCC≡CCOOH,M为HOOCCH(Cl)CH2COOH,
故答案为:HOOCCH(OH)CH2COOH;NaOOCCH=CHCOONa;HOOCC≡CCOOH;HOOCCH(Cl)CH2COOH;
(3)由上述分析可知,A→B属于消去反应; B→E属于加成反应,故答案为:消去反应;加成反应;
(4)M→A第①步卤代烃的水解反应反应,反应条件为:氢氧化钠水溶液、加热,
E→F第①步反应方程式为:HOOCCH(Br)CH(Br)COOH+4NaOH$→_{△}^{醇}$NaOOCC≡CCOONa+2NaBr+4H2O,
故答案为:氢氧化钠水溶液、加热;HOOCCH(Br)CH(Br)COOH+4NaOH$→_{△}^{醇}$NaOOCC≡CCOONa+2NaBr+4H2O;
(5)在催化剂作用下,HOOCCH=CHCOOH与乙二醇可发生缩聚反应,生成的高分子化合物用于制造玻璃钢.该反应的化学方程式为:n

故答案为:n

(6)与A具有相同官能团的A的同分异构体有: ,
,
故答案为: .
.
点评 本题考查有机物的推断,确定A的结构简式是关键,再结合反应条件与有机物分子式进行推断,侧重于学生的分析能力的考查,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY2Z3 | B. | X2YZ3 | C. | X3YZ4 | D. | X3YZ3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO4、H2SO4、H3PO4的酸性依次增强 | |
| B. | HCl、HBr、HI的稳定性依次增强 | |
| C. | 钠、镁、铝的还原性依次增强 | |
| D. | N、O、F原子半径逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 为防止粮食、罐头、水果等食品腐烂,常用氮气做保护气 | |
| B. | 酸雨的PH小于5.6 | |
| C. | SO2可以用作食物和干果的防腐剂 | |
| D. | 铵盐受热易分解,都生成氨气和对应的酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
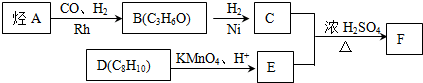

 .
.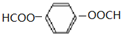 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含非极性键的分子一定是非极性分子 | |
| B. | 含有极性键的分子一定是极性分子 | |
| C. | 非极性分子一定含有非极性键 | |
| D. | 极性分子不一定只含有极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl | B. | MgO | C. | K2S | D. | NaF |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com