
【题目】下列说法正确的是
A.NaClO溶液中通入少量CO2,ClO﹣水解程度增大,溶液碱性增强
B.铁片镀锌时,铁片与外电源的正极相连
C.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)能自发进行,则ΔH<0
D.t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)![]() NO(g)+SO3(g),通入少量O2,
NO(g)+SO3(g),通入少量O2,![]() 的值及SO2转化率不变
的值及SO2转化率不变
科目:高中化学 来源: 题型:
【题目】为测定人体血液中Ca2+的含量,设计了如下方案:
![]()
有关反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4 K2SO4+2MnSO4+10CO2↑+8H2O若血液样品为15mL,滴定生成的草酸消耗了0.001mol·L-1的KMnO4溶液15.0mL,则这种血液样品中的含钙量为
A.0.001mol·L-1B.0.0025mol·L-1 C.0.0003mol·L-1D.0.0035mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气的主要成分是甲烷,含有少量的羰基硫![]() 、乙硫醇
、乙硫醇![]() 等气体。
等气体。
(1)组成羰基硫的元素中,原子半径最小的元素在周期表中的位置是 ______。
(2)乙硫醇有特殊气味,是天然气的臭味指示剂.乙硫醇可以看作是乙醇分子中羟基![]() 被
被![]() 取代,则乙硫醇的结构式为 ______。
取代,则乙硫醇的结构式为 ______。
(3)下列事实可用于比较C与S两种元素非金属性![]() 原子得电子能力
原子得电子能力![]() 相对强弱的是 ______ (填序号)。
相对强弱的是 ______ (填序号)。
a.沸点:![]()
![]() 元素在周期表中的位置
元素在周期表中的位置 ![]() 酸性:
酸性:![]()
![]() 同温同浓度水溶液的pH:
同温同浓度水溶液的pH:![]()
(4)羰基硫水解及利用的过程如下![]() 部分产物已略去
部分产物已略去![]() :
:![]() 溶液
溶液![]() 溶液
溶液![]()
①常温下,在反应Ⅱ中,每吸收![]() 气体放出热量a kJ,其热化学方程式为 ______。
气体放出热量a kJ,其热化学方程式为 ______。
②已知X溶液中硫元素的主要存在形式为![]() ,则反应Ⅲ中生成该离子的离子方程式为 ______。
,则反应Ⅲ中生成该离子的离子方程式为 ______。
③如图是反应Ⅲ中,在不同反应温度下,反应时间与![]() 产量的关系图
产量的关系图![]() 初始含量为
初始含量为![]() 请结合图象数据解释X溶液中除
请结合图象数据解释X溶液中除![]() 外,还有
外,还有![]() 、
、![]() 的原因______。
的原因______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2和N2O4可以相互转化:2NO2(g) ![]() N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法错误的是
N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法错误的是

A.图中共有两条曲线X和Y,其中曲线X表示NO2浓度随时间的变化
B.a、b、c、d四个点中,表示化学反应处于平衡状态的点是b和d
C.反应进行至25 min时,曲线发生变化的原因是加入0.4 mol N2O4
D.若要达到与d相同的状态,在25 min时还可以采取的措施是适当缩小容器体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁单质及化合物与我们的生产、生活紧密相关。
(1)Fe3+的基态核外价电子排布式为______,应用原子结构比较Fe与同周期的Mn第三电离能(I3)的大小:I3(Mn)_______I3(Fe)(填>、<、=)。理由是_______。
(2)Fe、Fe2+、Fe3+可以与CO、SCN-、CN-、H2NCONH2(尿素)等多种配体形成很多的配合物。
①配合物Fe(CO)5的熔点-20℃,沸点103℃,可用于制备纯铁。Fe(CO)5的结构如图所示:
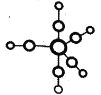
下列关于Fe(CO)5说法不正确的是________。
A.Fe(CO)5是分子晶体
B.Fe(CO)5中Fe原子的配体与C22-互为等电子体
C.Fe(CO)5中σ键与π键之比为1:1
D.Fe(CO)5=Fe+5CO反应中没有新化学键生成
②CN-的电子式为__________。
③H2NCONH2(尿素)中N、C原子的杂化方式分别为__________、__________,
组成尿素的4种元素的第一电离能由大到小的顺序为__________,1 mol H2NCONH2(尿素)分子中含有σ键的数目为__________。
(3)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3C,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是________。
(4)FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置的Fe或者b位置的Fe,形成Cu替代型产物Fe(x-n)CunNy,FexNy转化为两种Cu的替代型产物的能量变化如图2所示,其中相对不稳定的Cu替代型产物的化学式为__________。
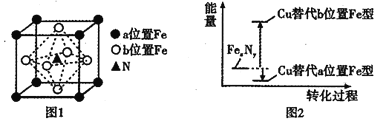
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小组同学查阅资料,得到了Na2CO3(aq)与盐酸反应过程中的能量变化示意图如下。
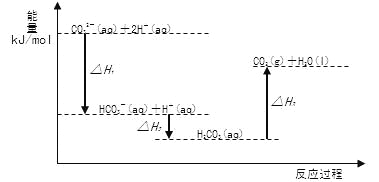
(注:碳酸钠与碳酸氢钠的溶解过程的热效应忽略不计)
下列说法错误的是
A.△H1<△H2
B.若反应HCO3-+H+=CO2↑+H2O的熵增效应大于吸热效应,则其在常温下能自发进行
C.CO32-(aq)+2H+(aq) =CO2(g)+H2O(l)△H=(△H1+△H2-△H3) kJ/mol
D.相同条件下,结合H+的能力:CO32->HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.4CuO(s)=2Cu2O(s)+O2(g)在室温下不能自发进行,说明该反应△H>0
B.向稀醋酸中加入醋酸钠固体,溶液pH升高的主要原因是醋酸钠水解呈碱性
C.室温下K(HCN)<K(CH3COOH),说明CH3COOH的电离度一定比HCN大
D.H2S(g)+FeO(s)![]() FeS(s)+H2O(g),其他条件不变时增大压强,反应速率V正(H2S)和H2S的平衡转化率均增大
FeS(s)+H2O(g),其他条件不变时增大压强,反应速率V正(H2S)和H2S的平衡转化率均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关仪器使用方法或实验操作正确的是![]()
A.洗净的锥形瓶和容量瓶可以放进烘箱烘干
B.酸式滴定管装标准溶液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差
D.用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃的锌猛干电池对环境污染很大,工业上可用如下工艺回收正极材料中的金属(部分条件未给出):

(1)MnO(OH)中Mn的化合价为__;实验室保存FeSO4溶液时为防止被氧化需加入__;实验室保存Fe2(SO4)3溶液时为抑制其水解应当加入__。
(2)加入H2O2的目的是将Fe2+氧化成Fe3+,则用离子方程式表示为___。
(3)该工艺流程中多次用到过滤,实验室中过滤所需要的玻璃仪器除烧杯外还有__。
(4)已知:25℃时,已知Ksp[Fe(OH)3]=1×10-38,当Fe3+浓度为1×10-5mol·L-1时,认为Fe3+沉淀完全,滤液1中加入NaOH溶液至pH=__时Fe3+沉淀完全。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com